2. 复旦大学附属华山医院检验科,上海 200040
2. Department of laboratory medicine, Huashan Hospital, Fudan University, Shanghai 200040
乙型肝炎e抗原(hepatitis B e antigen, HBeAg)由HBV前C区或C区编码而成,经由内质网-高尔基体结构分泌至胞外。HBeAg既不是HBV颗粒的结构成分,也不是HBV DNA复制所必需的,但是发生HBeAg血清学转换是免疫控制的指标,也是评估慢乙肝治疗疗效的重要指标。此外,血清HBeAg的水平反应了病毒的复制水平,且HBeAg对于维持乙型肝炎病毒(hepatitis B virus, HBV)的慢性感染至关重要。血清HBeAg与HBV DNA定量之间有显著相关性,即HBeAg阳性的患者绝大多数表现出HBV DNA阳性[1]。有研究表明,HBeAg阳性孕妇生产的子女即便接受了乙肝疫苗以及免疫球蛋白的阻断,相较于HBeAg阴性孕妇所生的子女而言,依旧具有较高的概率发生突破性HBV感染[2]。《亚太地区慢性乙型肝炎(CHB)治疗指南2012》里明确指出,HBeAg和HBV DNA均是乙肝患者监测的常规检测项目[3]。2015年3月发布的WHO首部全球慢性乙肝指南里也强调了定期监测慢性乙肝患者HBeAg指标的必要性[4]。尽管目前已有大量临床研究验证了HBeAg定量检测对临床诊疗的重要性,HBeAg的定量检测还未成为常规检验项目。为了将HBeAg定量检测应用于临床,本研究对HBeAg定量检测平台进行了性能验证,评估了定量检测和定性检测结果的相关性,并对慢性乙肝患者样本进行HBeAg定量检测,观察其与血清HBV DNA水平、丙氨酸氨基转移酶(alanine aminotransferase, ALT)、天冬氨酸氨基转移酶(aspartate aminotransferase, AST)等结果的相关性,为HBeAg定量检测在临床诊疗的应用提供实验依据。
1 资料和方法 1.1 一般资料标本来源为2019年3月至2019年5月来本院就诊的710例慢性乙型肝炎患者的血清。710例乙肝患者的HBeAg定性检测均为阳性,男性患者488例,女性患者222例,平均年龄(37.54±11.31)岁。根据血清学、病毒学和生物化学等检测结果有明确临床诊断的有98名患者,其中,78名患者处于免疫清除期,20名患者处于免疫耐受期[5]。关于98名患者的基线信息具体如表 1所示。本研究经复旦大学附属华山医院伦理委员会批准(编号:KY2015-212)。
| 项目 | 免疫耐受期(n=20) | 免疫清除期(n=78) | P值 |
| 男/女(人) | 8/12 | 65/13 | |
| 年龄(岁) | 32(30~37) | 34(23~58) | 0.548 |
| ALT (U/L) | 23(18~28) | 62(47.75~94) | < 0.000 1 |
| AST (U/L) | 20(19~25) | 42(31.25~55.75) | < 0.000 1 |
| HBsAg (logIU/ml) | 4.23(4.09~4.36) | 3.45(3.16~3.73) | < 0.000 1 |
| HBeAg (S/CO) | 781.84(22.00~1247.98) | 27.97(3.94~260.58) | 0.00 2 |
| HBeAg (pEIU/ml) | 189.36(2.47~426.90) | 4.24(0.44~53.91) | 0.003 |
| 注:P值< 0.05被认为有显著差异。数据以中位数(4分位间距)表示。 ALT: alanine aminotransferase; AST: aspartate aminotransferase; HBsAg: hepatitis B suface antigen | |||
本实验室首次使用雅培ARCHITECT HBeAg定量试剂在美国雅培ARCHITECT i4000SR全自动免疫分析仪上进行检测。因此,参照美国临床实验室标准化协会(CLSI)相关指南文件EP10A3,对HBeAg定量检测系统的精密度、分析灵敏度、线性范围/可报告范围、携带污染率进行分析和验证,来评估其检测性能是否满足实验室的常规使用要求。验证期间,已确认仪器运转良好,质控在控。
1) 精密度验证实验
取两个浓度的质控品作为验证材料连续检测5天,各浓度每天重复测定5次。每浓度水平获得25个数据。若计算的精密度小于等于厂商声明的质量要求,则验证通过。
2) 分析灵敏度验证实验
将ARCHITECT HBeAg定量手工稀释液作为“0”浓度样品,连续测定20次,重复测定已知浓度样本(0.7 PEIU/mL)3次,记录“0”浓度和已知浓度测定结果的相对光单位(relative light unit, RLU)值。如果计算的分析灵敏度≤厂家声明,则验证通过。
3) 线性范围
厂商声明的线性范围是1~700 PEIU/mL,取已知浓度的患者高值(H)、低值(L)标本各一份(高值标本浓度为696 PEIU/mL,低值标本浓度为2 PEIU/mL)。将L和H按照如下方式进行配比:5L+0H,4L+1H,3L+2H,2L+3H,1L+4H,0L+5H,组成6份验证物质。测定该验证物质浓度,每份重复测定2次。线性可允许系统误差要求≤1/2 TEA,TEA=25%。
4) 携带污染率
取高浓度样本(H)和低浓度样本(L)各一份,将高浓度样本分成10份,低浓度样本分成11份,21份样本按顺序:L1-L2-L3-H1-H2-L4-H3-H4-L5-L6-L7-L8-H5-H6-L9-H7-H8-L10-H9-H10-L11连续测定。携带污染=High-Low的均值-Low-Low的均值,即(L4+L5+L9+L10+L11)/ 5-(L2+L3+L6+L7+L8) / 5,携带污染 < 3倍Low-Low的SD则验证通过。
1.2.2 HBeAg定性测定本实验室HBV血清标志物检测常规采用美国雅培ARCHITECT i4000SR全自动免疫分析仪以及乙型肝炎病毒e抗原测定试剂盒。患者血清样本经实验室常规HBeAg定性检测之后,结果判定阳性标准为HBeAg S/CO值≥1.0,HBeAg S/CO值< 1.0为阴性。
1.2.3 HBeAg定量测定取HBeAg定性检测结果判定为阳性的患者样本,采用美国雅培ARCHITECT i4000SR全自动免疫分析仪、乙型肝炎病毒e抗原测定试剂盒和乙型肝炎病毒e抗原校准品。HBeAg定量检测结果以Paul Ehrlich institute单位(PEIU/mL)表示。
1.3 HBV DNA定量测定取HBeAg定性检测为阳性的患者样本,采用美国Applied Biosystems公司的7500 Real Time PCR System和上海科华公司的乙型肝炎病毒核酸测定试剂盒。质控品来自上海市临床检验中心。HBV DNA阳性标准:HBV DNA>5×102Copy/mL。
1.4 统计学处理HBeAg定量检测的性能验证数据采用EP Evaluation @软件(Release11)进行分析。HBeAg定量和定性检测、HBeAg定量和HBV DNA定量检测结果的分别比对,采用MedCalc(version 19.1)统计软件进行统计分析,利用配对T检验和Passing-Bablok回归分析比较两种方法检测结果的相关性。P < 0.05被认为差异有统计学意义。
2 结果 2.1 HBeAg定量检测的性能验证精密度验证计算低值均值为1.335 PEIU/mL,批内精密度为2.7%,小于说明书宣称的5.25%,总精密度为5.2%,小于说明书中的7.04%,验证通过; 精密度高值均值为99.387 PEIU/mL,高值批内精密度为1.5%,小于说明书的3.03%,总精密度为4.7%,小于说明书中的5.58%,验证也通过。灵敏度验证的数据经统计计算得灵敏度为0.014 PEIU/mL,小于厂商声明的0.02 PEIU/mL,验证通过。线性范围/可报告范围验证结果经统计分析,线性验证误差(error)为7.0%,小于线性可允许系统误差12.5%,且在检测的0~619.520 PEIU/mL范围内成线性,验证通过。携带污染率数据经统计评估为0.010,符合厂家声明和本院要求,验证通过。因此,经过验证,ARCHITECT HBeAg定量检测系统的精密度、分析灵敏度、线性范围、携带污染率均符合需求。
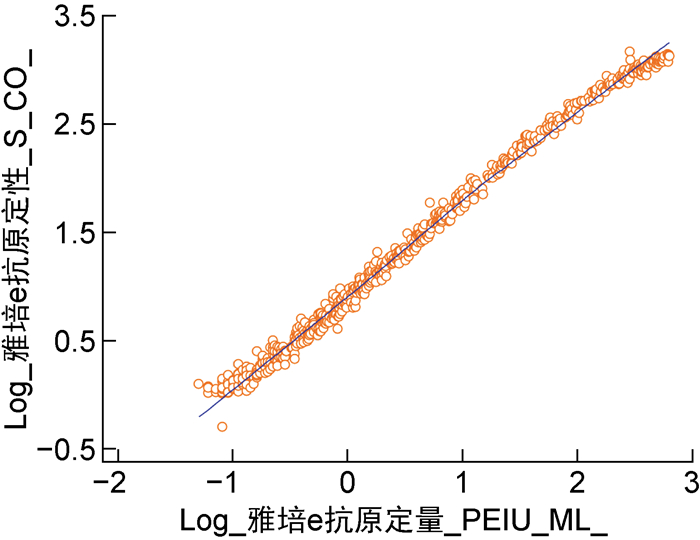
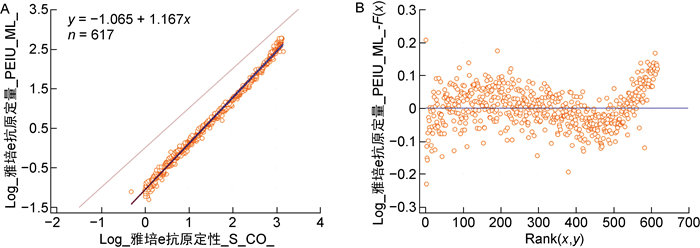
2.2 HBeAg定性和定量检测比对分析性能验证显示HBeAg定量检测在0~619.520 PEIU/mL范围内成线性,因此选取HBeAg定量检测值在线性范围内的样本共618例来对比分析HBeAg定量和定性的检测结果。两种方法的检测结果均取Log10之后用对数值做统计分析。配对t检验显示HBeAg定量和定性检测方法的相关性良好(r=0.997,P < 0.000 1),如图 1所示。Passing Bablok回归分析的回归方程为y=-1.064+1.167x (r=0.997,P < 0.000 1,95%CI=0.997~ 0.998),显示相关性良好, 具体如图 2所示。
|
| 图 1 HBeAg定性和定量检测的相关性 Fig. 1 Correlation between qualitative and quantitative HBeAg detection |
|
| 图 2 Passing Bablok回归分析HBeAg定量和定性检测的一致性 Fig. 2 Consistency of quantitative and qualitative HBeAg detection with Passing Bablok regression analysis |
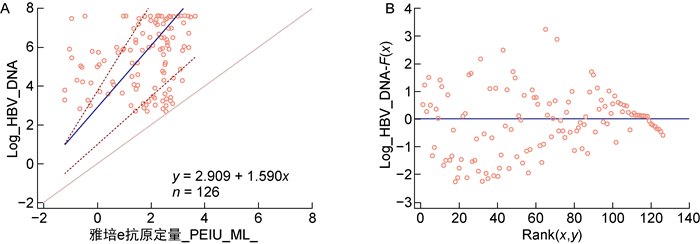
选取126例同时定量检测了HBeAg和HBV DNA的样本,运用Passing and Bablok回归分析两种方法的相关性,回归方程为y=2.909+1.590x (r=0.363,P < 0.000 1,95%CI=1.009~ 3.765),显示HBeAg定量与HBV DNA定量检测水平呈明显的正相关,由表中统计可知,随着HBeAg定量水平的升高,处于高病毒载量的人群占比越来越高(见表 2和图 3)。
| HBeAg (PEIU/ml) | n | HBV DNA(IU/ml) | |||||
| < 103 | 103~104 | 104~105 | 105~106 | 106~107 | >107 | ||
| < 0.1 | 2 | 0(0) | 2(100) | 0(0) | 0(0) | 0(0) | 0(0) |
| 0.1~10 | 27 | 2(7.4) | 4(14.8) | 7(25.9) | 11(40.7) | 0(0) | 3(11.1) |
| 10~100 | 27 | 4(14.8) | 4(14.8) | 4(14.8) | 3(11.1) | 6(22.2) | 6(22.2) |
| 100~1 000 | 55 | 3(5.5) | 12(21.8) | 4(7.3) | 6(10.9) | 11(20) | 19(34.5) |
| >1 000 | 14 | 0(0) | 0(0) | 2(14.3) | 2(14.3) | 2(14.3) | 8(57.1) |
|
| 图 3 Passing-Bablok回归分析HBeAg定量和HBV DNA定量检测的相关性 Fig. 3 Correlation between quantification of HBeAg and HBV DNA using Passing-Bablok regression analysis |
在98名有明确临床诊断的患者中选取有HBV DNA检验数据的57名患者,根据HBeAg定量水平分为0.1~1.3 PEIU/mL,1.3~20 PEIU/mL,20~250 PEIU/mL,≥250 PEIU/mL 4组, 由表中数据统计可知,随着HBeAg定量检测值的逐渐升高,HBV DNA病毒载量结果也相应增加。当HBeAg定量高于250 PEIU/ml时,可检测的HBV DNA的比率升高(46.15%升至83.33%),ALT或AST异常率显著降低(92.31%降至50.00%)(见表 3)。
| HBeAgPEIU/ml | N | Detectable HBV DNA | ALT(U/L) median(IQR) | AST(U/L) median(IQR) | ALT or ASTAbnormal Rate (%) | |||
| Rate(%) | Valuea | |||||||
| 0.1~1.3 | 16 | 18.75 | 4.3±1.09 | 58 | (44~72) | 37 | (27~50) | 81.25 |
| 1.3~20 | 16 | 25.00 | 5.4±0.76 | 49 | (45~78) | 40 | (28~47) | 87.50 |
| 20~250 | 13 | 46.15 | 5.0±2.09 | 62 | (49~89) | 40 | (24~52) | 92.31 |
| ≥250 | 12 | 83.33 | 5.3±1.74 | 43 | (25~126) | 27 | (19~73) | 50.00 |
| a数据为平均值±标准差(log10IU/ml)。 | ||||||||
随着医疗研究的进展和医疗技术的不断进步, HBV血清学标志物的检测从定性检测进步到了定量检测[6-12],定量检测使得一些乙肝血清学指标有了新的临床意义和应用,如HBsAg定量检测已经被纳入《慢性乙型肝炎防治指南》(2015年版),为乙肝诊疗个体化提供了新的依据[4]。近年来,关于HBeAg定量检测与慢性乙型肝炎治疗疗效的相关研究越来越多。一项关于接受干扰素治疗的HBeAg阳性慢性乙型肝炎患者的回顾性研究,对比了HBV DNA和HBeAg对于治疗后6个月HBeAg血清学转换的预测价值,发现:在干扰素治疗24周时,HBeAg、HBV DNA水平均可预测治疗后6个月的持久应答,且HBeAg比HBV DNA能更好地预测HBeAg的血清学转换; HBeAg水平在干扰素治疗24周处于低中值(< 100 PEIU/mL)时,其预测价值和HBV DNA没有明显差别,但是水平处于高值(>100 PEIU/mL)时,HBeAg的预测值远高于HBV DNA(96% vs 86%)。这项研究结果表明血清HBeAg的定量检测可以用来补充或者部分替代HBV DNA作为HBeAg阳性乙肝患者干扰素治疗监控的指标[13]。慢性乙型肝炎患者治疗过程中的HBeAg定量水平变化,也是预测核苷(酸)类似物(nucleoside/nucleotide analogues, NAs) 治疗反应的有效工具。一项前瞻性研究纳入76例HBeAg阳性慢性乙型肝炎患者接受96周核苷(酸)类似物治疗,分别于治疗前、治疗后12周、24周定量监测血清HBV表面抗原(HBV surface antigen, HBsAg)、HBeAg、乙型肝炎核心抗体(hepatitis B core antibody, HBcAb)、HBV DNA和ALT的水平,结果显示治疗24周的HBeAg指标下降水平和幅度可用来预测病毒学应答和血清转换[14]。
HBeAg是诊断有无HBV感染和传染性的常用血清标志物。目前临床主要应用酶免疫法或化学发光法来检测HBeAg,判断阴阳性,用于辅助诊断HBV的感染状态[15-17]。HBeAg定性检测相较于定量检测具有检测快速、经济等优点,在筛查乙型肝炎患者中发挥了重要作用,但是在评估及预测HBeAg阳性慢性乙型肝炎患者治疗疗效方面差于定量检测。近年来,随着免疫技术的发展和应用,HBeAg定量检测已经成为临床研究常用的指标。HBeAg和HBV DNA一起被纳入《慢性乙型肝炎防治指南》(2015年版),作为判断HBV治疗转归的标志。本实验室验证了雅培ARCHITECT i4000SR全自动免疫分析仪最新的HBeAg定量检测分析性能,验证结果表明HBeAg定量检测的精密度、分析灵敏度、线性范围、携带污染率均符合厂家说明书和本实验室的要求。通过对比慢性乙型肝炎患者HBeAg定性和定量两种检测方法的结果,发现这两种检测方法具有良好的相关性。本研究也验证了HBeAg定量检测结果和HBV DNA的检测结果呈正相关且当HBeAg定量≥250 PEIU/ml时,可检测的HBV DNA的比率升高(46.15%升至83.33%),ALT或AST异常率显著降低(92.31%降至50.00%)。基于HBV DNA与HBeAg的定量检测结果的相关性,可由HBeAg定量结果对HBV DNA进行初步预测,并且当HBeAg≥250 PEIU/ml时,ALT或AST的异常率显著降低,ALT或者AST水平与肝脏的炎症活动密切相关,对临床诊断和治疗有一定的指导意义。综上所述,HBeAg可以用于实验室的常规检测来为临床乙型肝炎患者诊疗提供依据。
| [1] |
Chen P, Xie Q, Lu X, Yu C, Xu K, Ruan B, Cao H, Gao H, Li L. Serum HBeAg and HBV DNA levels are not always proportional and only high levels of HBeAg most likely correlate with high levels of HBV DNA: a community-based study[J]. Medicine (Baltimore), 2017, 96(33): e7766.
[DOI]
|
| [2] |
Chen HL, Lin LH, Hu FC, Lee JT, Lin WT, Yang YJ, Huang FC, Wu SF, Chen SC, Wen WH, Chu CH, Ni YH, Hsu HY, Tsai PL, Chiang CL, Shyu MK, Lee PI, Chang FY, Chang MH. Effects of maternal screening and universal immunization to prevent mother-to-infant transmission of HBV[J]. Gastroenterology, 2012, 142(4): 773-781.e2.
[DOI]
|
| [3] |
Liaw Y-F, Kao J-H, Piratvisuth T, Chan HLY, Chien R-N, Liu C-J, Gane E, Locarnini S, Lim S-G, Han K-H, Amarapurkar D, Cooksley G, Jafri W, Mohamed R, Hou J-L, Chuang W-L, Lesmana LA, Sollano JD, Suh D-J, Omata M. Asian-Pacific consensus statement on the management of chronic hepatitis B: a 2012 update[J]. Hepatol Int, 2012, 6(3): 531-561.
[DOI]
|
| [4] |
World Health Organization. Guidelines for the Prevention, Care and Treatment of Persons with Chronic Hepatitis B Infection[M]. Geneva, Switzerland: WHO Press, 2015.
|
| [5] |
王贵强, 段钟平, 王福生, 庄辉, 李太生, 郑素军, 赵鸿, 侯金林, 贾继东, 徐小元, 崔富强, 魏来. 慢性乙型肝炎防治指南(2019年版)[J]. 实用肝脏病杂志, 2020, 23(1): S9-S32. [CNKI]
|
| [6] |
Chu C-J, Hussain M, Lok ASF. Quantitative serum HBV DNA levels during different stages of chronic hepatitis B infection[J]. Hepatology, 2002, 36(6): 1408-1415.
[DOI]
|
| [7] |
Fu X, Tan D, Dou X, Chen J, Wu J. A multi-center clinical study comparing Sansure Magb and CAP/CTM HBV tests in the quantitative detection of HBV DNA[J]. J Infect Dev Ctries, 2016, 10(7): 755-761.
[DOI]
|
| [8] |
Cornberg M, Wong VW, Locarnini S, Brunetto M, Janssen HLA, Chan HL. The role of quantitative hepatitis B surface antigen revisited[J]. J Hepatol, 2017, 66(2): 398-411.
[DOI]
|
| [9] |
王林, 刘学恩, 庄辉. 乙型肝炎病毒核心相关抗原定量检测的临床意义[J]. 中国病毒病杂志, 2019, 9(1): 24-32. [CNKI]
|
| [10] |
王蕾, 李世宝, 金玉. 乙型肝炎血清标志物模式及前S1抗原与乙型肝炎病毒DNA定量检测的关系[J]. 临床与病理杂志, 2018, 38(10): 2088-2093. [CNKI]
|
| [11] |
Piermatteo L, Salpini R, Alkhatib M, Bertoli A, Iuvara A, De Cristofaro M, Cappiello G, Cerva C, Minichini C, Pisaturo M, Starace M, Coppola N, Fontana C, Sarmati L, Andreoni M, Angelico M, Grelli S, Ceccherini Silberstein F, Perno CF, Svicher V. Quantitative HBeAg varies across the different phases of HBV infection, and can predict treatment outcome in the setting of HBV-reactivation driven by iatrogenic immunosuppression[J]. Digest Liver Dis, 2020, 52(Supl1): e21-e22.
|
| [12] |
朱萍, 路毓峰, 王丽, 王红, 杨莉, 卢建华, 李敏然, 叶立红, 陈秀丽. 肝脏组织炎症程度与血清HBeAg定量的相关性研究[J]. 临床荟萃, 2019, 34(7): 637-640. [CNKI]
|
| [13] |
Fried MW, Piratvisuth T, Lau GK, Marcellin P, Chow WC, Cooksley G, Luo KX, Paik SW, Liaw YF, Button P, Popescu M. HBeAg and hepatitis B virus DNA as outcome predictors during therapy with peginterferon alfa-2a for HBeAg-positive chronic hepatitis B[J]. Hepatology, 2008, 47(2): 428-434.
[DOI]
|
| [14] |
Gao YH, Meng QH, Zhang ZQ, Zhao P, Shang QH, Yuan Q, Li Y, Deng J, Li T, Liu XE, Zhuang H. On-treatment quantitative hepatitis B e antigen predicted response to nucleos(t)ide analogues in chronic hepatitis B[J]. World J Hepatol, 8(34): 1511-1520. doi: 10.4254/wjh.v8.i34.1511.
|
| [15] |
Si J, Li J, Zhang L, Zhang W, Yao J, Li T, Wang W, Zhu W, Allain JP, Fu Y, Li C. A signal amplification system on a lateral flow immunoassay detecting for hepatitis e-antigen in human blood samples[J]. J Med Virol, 2019, 91(7): 1301-1306.
[DOI]
|
| [16] |
Huang R, Xi Z, Deng Y, He N. Fluorescence based Aptasensors for the determination of hepatitis B virus e antigen[J]. Sci Rep, 2016, 6: 31103.
[DOI]
|
| [17] |
Gao Z, Li Y, Zhang X, Feng J, Kong L, Wang P, Chen Z, Dong Y, Wei Q. Ultrasensitive electrochemical immunosensor for quantitative detection of HBeAg using Au@Pd/MoS2@MWCNTs nanocomposite as enzyme-mimetic labels[J]. Biosens Bioelectron, 2018, 102: 189-195.
[DOI]
|
 2021, Vol. 16
2021, Vol. 16


