星座链球菌(Streptococcus constellatus) 是一种条件致病菌,在机体抵抗力下降时可引起全身各个器官,包括胸膜腔、颈部、肝脏、腰大肌、硬脊膜、淋巴结、甲状腺等部位的化脓性感染[1],但目前致脑脓肿极为少见,而中、外文文献均为个案报道[2-3]。本实验室从就诊于本院的1例患者脑脓肿组织中分离出星座链球菌,报道如下。
1 临床材料 1.1 病例患者,男性,56岁,农民。头痛3个月,视物成双19天,发热5天。患者于3个月前低头感觉左侧头痛,呈发作性,能自行缓解,症状持续1周后头痛加重,左侧后枕部至前额部呈搏动性胀痛,伴有左眼胀痛,严重时左侧流泪、流涕,头颈部出汗。在当地县医院就诊,均按颈椎病治疗。入我院19天前间断视物成双,11天前到当地市立医院就诊,行颅脑磁共振成像(magnetic resonance imaging,MRI)及强化扫描,显示左侧小脑半球长T1、长短T2, T2FLAIR高低信号,增强后多房样环形强化。左侧海绵窦异常信号并强化,不排除转移瘤、炎性病变。行胸、腹部电子计算机断层扫描(computed tomography,CT),未见明显异常。5天前患者疼痛时出现发热,最高38.3 ℃,腰椎穿刺示脑压23.3 kPa,脑脊液白细胞4.7×108/L,单核细胞比例90%,多核细胞比例10%。在当地市立医院住院10天,给予甘露醇脱水,头孢曲松抗感染,症状无明显缓解。为进一步治疗,患者来我院就诊。
入院后复查MRI,显示:①海绵窦左侧异常强化灶伴有蝶窦后壁黏膜增厚,考虑炎性病变并左侧小脑半球脓肿形成;②双侧额叶皮层下小缺血灶,与前次比较,左侧小脑病灶增大,并包裹成球形,数量也较前增多。腰椎穿刺取脑脊液复查,结果显示:白细胞5.4×107 /L,较前下降,其中淋巴细胞比例93%,中性粒细胞为7%;蛋白0.83 g/L,较前上升;氯110.0 mmol/L,较前下降。影像学复查结果提示:不排除结核感染形成的结核球,建议予以抗结核治疗。但该病例结核感染T细胞检测为阴性,并不支持结核杆菌既往感染。
患者既往病史:有糖尿病史2年半,胰岛素治疗。患者有明显的牙周疾病,右侧上颌多个牙齿缺失,近期左侧上颌疼痛明显。否认有冠心病、高血压等慢性病史。否认肝炎、结核等急、慢性传染病史及接触史。入院查体:体温36.5 ℃,血压14.0/9.3 kPa,呼吸频率16次/分,脉搏70次/分。患者自发病以来,神志差,饮食不规律,大、小便无异常。全身皮肤及黏膜无黄染,未见皮疹、紫癜及出血点。双肺呼吸音清,未闻及干、湿啰音。心律齐,心音有力,各瓣膜听诊区未闻及病理性杂音。神经系统体格检查无异常。血常规检查:白细胞7.67×109/L,中性粒细胞4.83×109 /L,血红蛋白134 g/L,血小板4.09×1011/L。肝功能未见明显异常。空腹血糖8.68 mmol/L,血沉36 mm/h。脑脊液生化检查:腺苷脱氨酶2.0 U/L,氯110 mmol/L,葡萄糖4.61 mmol/L,蛋白0.87 g/L。脑脊液常规检查:脑脊液白细胞1.42×108/L,淋巴细胞比例96%,中性粒细胞比例4%。乙型肝炎表面抗原、丙型肝炎抗体、梅毒抗体、HIV抗体等传染病指标均为阴性。
初步诊断:小脑多发性脓肿;2型糖尿病。
1.2 材料和方法 1.2.1 主要试剂哥伦比亚血琼脂培养基、巧克力色琼脂培养基、麦康凯琼脂培养基、革兰氏染色液均购自济南百博生物技术股份有限公司。
1.2.2 宏基因组测序取患者脑脊液送华大基因进行宏基因组测序。将所得测序数据经过处理后,与微生物大数据库比对,根据序列数的高低及临床信息判断可能的病原体。
1.2.3 组织标本的细菌培养将脑脓肿组织标本分别接种于哥伦比亚血琼脂培养基、巧克力色琼脂培养基、麦康凯琼脂培养基,将平板置于35 ℃、5% CO2培养箱中培养24 h。
1.2.4 显微镜镜检将脑脓肿组织研磨后直接涂片,取脑脓肿组织24 h培养物进行涂片,分别革兰染色后镜检。
1.2.5 基质辅助激光解吸电离飞行时间质谱技术(matrix-assisted laser desorption/ ionization time of flight mass spectrometry,MALDI-TOF-MS)检测用甲酸提取法进行样本前处理。使用FlexControl 3.4软件采集图谱。使用BioTyper 3.1软件对所得图谱在仪器数据库内进行比对。
1.2.6 药物敏感性试验根据美国临床和实验室标准协会(Clinical and Laboratory Standards Institute,CLSI)建议的α-溶血链球菌药敏组合,使用纸片扩散法(K-B法)对脑脓肿组织培养细菌进行药敏鉴定。药物敏感性判定采用CLSI在2020年发布的《M100-Performance Standards for Antimicrobial Susceptibility Testing, 30 st Edition》中的药敏折点标准为依据。使用的抗生素包括青霉素G、头孢噻肟、头孢曲松、万古霉素、头孢吡肟以及利奈唑胺。
2 结果 2.1 脑脊液宏基因组测序提示细菌感染脑脊液宏基因组测序结果显示为直肠弯曲菌、福赛斯坦纳菌和棘孢木菌。查阅文献发现有直肠弯曲菌引起颅内脓肿的报道,遂停用抗结核治疗,改用莫西沙星抗菌治疗。患者头痛不适加重,双上眼睑浮肿明显,双眼左侧受限,再次复查MRI,提示病灶逐步扩大,病情变化较快,外周血白细胞10.79×109/L,中性粒细胞79.8%,血小板388×109/L。将患者转神经外科,急诊行小脑占位性病变清除术,术中明确为脑脓肿,术后给予止血、抗感染、脱水降颅压、解热镇痛、控制血糖、营养支持等综合治疗方案。术后观察脓性组织,提示为肉芽组织增生伴大量急、慢性炎性细胞浸润,局部脓灶形成。
2.2 革兰染色镜检阴性脑脓肿组织研磨后直接涂片,镜下未见可疑病原菌。
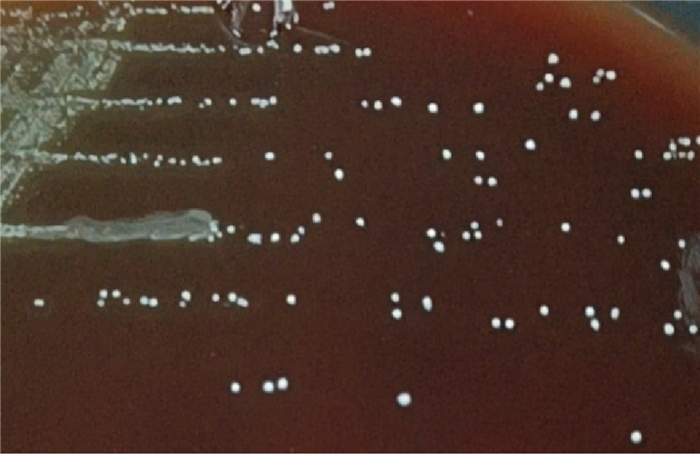
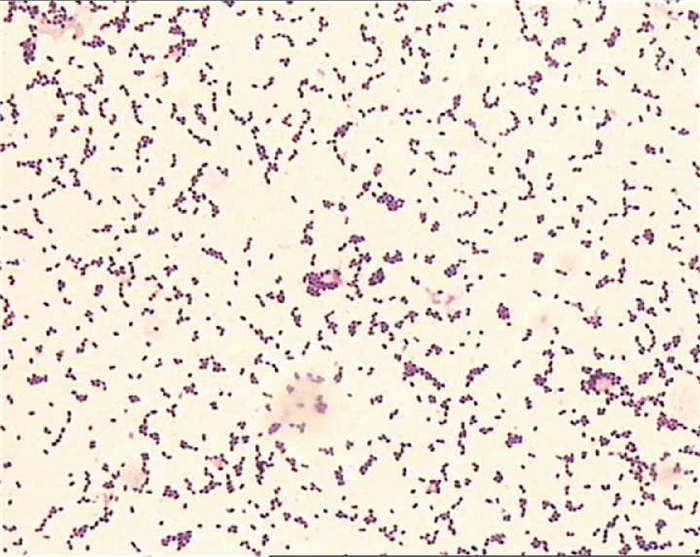
2.3 脑脓肿组织培养检出星座链球菌脑脓肿组织接种培养24 h后,可见α-溶血的针尖样小菌落,菌落大小1 mm,呈白色凸起(见图 1)。取该菌落涂片后革兰染色,镜下可见革兰阳性球菌呈链状排列(见图 2)。用MALDI-TOF法鉴定该菌,结果显示为星座链球菌,分值为1.97。根据2020年CLSI发布的《M100-Performance Standards for Antimicrobial Susceptibility Testing, 30 th Edition》对星座链球菌进行药敏试验,参考药敏结果(具体见表 1)用利奈唑胺抗感染治疗,经综合治疗后,患者病情平稳出院。出院后继续静脉输注利奈唑胺1个月。随访提示患者恢复情况良好。
|
| 图 1 患者脑脓肿组织培养24 h的菌落形态 Fig. 1 Colonial morphology at 24 hours of incubation (from patient's brain tissue with abscess) |
|
| 图 2 革兰染色下的细菌形态(100×10) Fig. 2 Bacterial morphology displayed by gram staining |
| 抗菌药物 | 敏感度 | K-B(mm) | 折点(mm) | |
| 耐药 | 敏感 | |||
| 青霉素G | 33 | |||
| 头孢噻肟 | 敏感 | 28 | ≤25 | ≥29 |
| 头孢曲松 | 敏感 | 28 | ≤24 | ≥27 |
| 万古霉素 | 敏感 | 21 | ≥17 | |
| 头孢吡肟 | 敏感 | 28 | ≤21 | ≥24 |
| 利奈唑胺 | 敏感 | 28 | ≥21 | |
星座链球菌为革兰阳性球菌,属米勒链球菌组,一般分布于口腔、胃肠道和泌尿生殖道等部位,通常情况下不致病。但少数情况下,特别是当机体免疫功能下降时,星座链球菌可作为病原菌引起全身各组织器官感染[4]。星座链球菌可导致门静脉多发血栓形成[5]、肺部感染合并血流感染[6]以及脓胸[7]等。根据微生物培养的标本类型,才能确定星座链球菌是否为致病菌。本病例中,从脑组织中分离出星座链球菌,属于从无菌部位分离出细菌,致病菌的可能性大。同时,由于标本是脑脓肿组织,在培养的过程中采取了需氧环境和厌氧环境相结合的培养方式,结果两种培养条件下都有菌落生长。经过质谱鉴定,均为星座链球菌。这提示组织或无菌体液标本需要注意厌氧环境下细菌的培养。因为体内正常菌群的存在,导致很多厌氧菌都是条件致病菌。
星座链球菌是口腔颌面部间隙感染的重要病原菌之一[8]。本病例中,患者有明显的牙周病,根据宏基因组测序结果,曾怀疑其脑脓肿由牙周致病菌中的直肠弯曲菌引起。但是使用抗直肠弯曲菌的莫西沙星治疗效果不好,病情加重。用脑脓肿组织进行细菌培养,经过质谱鉴定是星座链球菌。根据星座链球菌的药敏结果给予利奈唑胺抗感染治疗,患者恢复良好。根据治疗结果,我们推测该患者的脑脓肿很可能是由牙周感染引发,致病菌是星座链球菌,而非直肠弯曲菌。当然,要直接证明患者脑脓肿是由来自口腔的星座链球菌引发,还应进行口腔分泌物培养,若也能分离出星座链球菌并测序证实,则可进一步证明是由于牙周感染导致口腔的星座链球菌引发脑脓肿。但是,该患者已痊愈出院,无法取到口腔分泌物的标本,所以仅能根据病史和临床治疗效果进行推测。Akashi等[3]也曾报道过3例牙源性感染的脑脓肿病例。其中1例脑脓肿的致病菌是金黄色葡萄球菌,第2例是星座链球菌、具核梭菌和微小微单胞菌混合感染,第3例是乳酸杆菌、牙龈卟啉单胞菌和聚合梭杆菌混合感染。这3例由牙源性细菌引发脑脓肿的病例与本报道的病例具有一定的一致性。在本病例中,除了使用利奈唑胺抗感染外,小脑占位性病变清除术对清除感染病灶也非常重要。徐龙彪等[2]曾报道星座链球菌所致脑脓肿1例,在其报道的病例讨论中,充分肯定了手术对清除脑脓肿的重要性。
以二代测序(next generation sequescing, NGS)为基础的宏基因组测序技术能对样品中的全部微生物DNA进行测序分析,具有无偏倚的优点,可检测出一些传统病原学培养方法无法检测的微生物,或者用来探究某种已知微生物的未知致病能力或做毒力判断。宏基因组测序技术在病原微生物感染的诊断中正起到越来越重要的作用[9-11]。Lin等[12]通过依赖/非依赖培养的宏基因组测序技术检测了脑脓肿中各种病原体的存在,包括细菌、真菌和病毒;而在以培养物为基础的宏基因组测序结果中,发现了一种名为普雷沃菌属(Prevotella)的新型细菌以及高GC含量的星座链球菌。有文献报道,宏基因组测序技术可检测出口腔来源并导致脑膜炎的致病菌[13]。但是,宏基因组测序技术应用于临床还处于经验积累期,Brown等[14]建议,对于慢性和反复发作的脑炎,可把宏基因组测序作为一线诊断手段;而在急性脑炎中将宏基因组作为二线检测手段。在本病例中,宏基因组测序结果与实际组织培养的结果并不相符。从治疗效果看,在手术基础上,依靠传统病原学培养方法,根据组织培养出的细菌及其药敏结果对患者进行治疗,可使患者转危为安。宏基因组测序技术在急性脑炎病原菌的诊断中,仅能作为二线检测手段,这也与Brown的建议相符。就本病例而言,宏基因组测序技术在急性神经病变的诊断中有其适用范围,宏基因组测序结果可作为参考,但一定要结合临床症状灵活处理感染病例。另外,张梦瑶等[15]在综述中指出,脑脊液的宏基因组测序有假阴性的情况。由于脑脊液中病原体效价低,容易导致宏基因组测序假阴性,与常规微生物培养阳性结果不一致。牛分枝杆菌、结核分枝杆菌、隐球菌、痤疮丙酸杆菌、梭形芽孢杆菌等病原体感染时都可能存在这种不一致的情况。
综上分析,作为一种口腔颌面部常见感染菌,星座链球菌有可能引发脑脓肿,这应引起临床工作者的注意。对于免疫力低下的患者,一定注意保持口腔卫生,避免星座链球菌经口腔引起脑脓肿。
| [1] |
曾桓超, 方志成, 杨贤义. 星座链球菌感染致气管-纵隔-胸膜瘘一例[J]. 中国急救复苏与灾害医学杂志, 2020, 12(15): 1471-1472. |
| [2] |
徐龙彪, 黄李法, 赵明. 星座链球菌致脑脓肿1例[J]. 温州医科大学学报, 2016, 46(8): 620-621. [DOI]
|
| [3] |
Akashi M, Tanaka K, Kusumoto J, Furudoi S, Hosoda K, Komori T. Brain abscess potentially resulting from odontogenic focus: report of three cases and a literature review[J]. J Maxillofac Oral Surg, 2017, 16(1): 58-64.
[DOI]
|
| [4] |
徐涛, 王华英, 俞万钧. 结核病合并星座链球菌感染2例及文献复习[J]. 中华全科医学, 2018, 16(9): 1588-1590. [CNKI]
|
| [5] |
刘贤贤, 田文超, 丁国锋, 成金英, 李冬梅. 星座链球菌血流感染致门静脉多发血栓形成1例[J]. 中国感染与化疗杂志, 2020, 20(4): 430-432. [CNKI]
|
| [6] |
刘琴, 冯习坤. 星座链球菌致肺部感染合并血流感染1例[J]. 安徽医药, 2018, 22(8): 1556-1557. [DOI]
|
| [7] |
蔡丽婷, 田家伟, 侯昕珩. 星座链球菌脓胸2例[J]. 中国感染与化疗杂志, 2021, 21(2): 205-207. [CNKI]
|
| [8] |
王静静, 郭丽芳, 王芳, 霍玉青. 口腔颌面部间隙感染病原菌与耐药性[J]. 中华医院感染学杂志, 2020, 30(20): 3142-3145. [CNKI]
|
| [9] |
郭凌云, 李勤静, 刘钢. 宏基因组测序技术在中枢神经系统感染病原体检测中的应用现状[J]. 中华传染病杂志, 2019, 37(5): 314-317. |
| [10] |
纪洪艳, 王国平, 郭切, 周长凯, 张传洲, 杨雪, 梁瑜. 应用宏基因组二代测序方法确诊的Q热心内膜炎一例[J]. 中华内科杂志, 2021, 60(3): 247-248. |
| [11] |
Gu W, Miller S, Chiu CY. Clinical metagenomic next-generation sequencing for pathogen detection[J]. Annu Rev Pathol, 2019, 14: 319-338.
[PubMed]
|
| [12] |
Lin JH, Wu ZY, Gong L, Wong CH, Chao WC, Yen CM, Wang CP, Wei CL, Huang WT, Liu PY. Complex microbiome in brain abscess revealed by whole-genome culture-independent and culture-based sequencing[J]. J Clin Med, 2019, 8(3): 351.
[DOI]
|
| [13] |
Heintz E, Pettengill MA, Gangat MA, Hardy DJ, Bonnez W, Sobhanie MM. Oral flora meningoencephalitis diagnosis by next-generation DNA sequencing[J]. Access Microbiol, 2019, 1(9): e000056.
[DOI]
|
| [14] |
Brown JR, Bharucha T, Breuer J. Encephalitis diagnosis using metagenomics: application of next generation sequencing for undiagnosed cases[J]. J Infect, 2018, 76(3): 225-240.
[PubMed]
|
| [15] |
张梦瑶, 任建发, 陈亚南, 邸卫英. 脑脊液宏基因组二代测序技术及其在中枢神经系统感染性疾病诊断中的应用进展[J]. 山东医药, 2020, 60(27): 86-90. [CNKI]
|
 2021, Vol. 16
2021, Vol. 16


