2021年以来,新型冠状病毒肺炎(以下简称“新冠”)疫情仍在世界范围内肆虐,截至10月24日,全球新冠病例数超2.43亿、死亡数超494万① (网址:https://covid19.who.int/table)。因多种传染性增强的新冠病毒变异株广为流行,且部分国家和民众防控松懈等原因,新冠疫情在许多国家及地区首次或多次暴发。新冠疫苗被批准推广使用后效果显著,高比例接种国家及地区的疫情态势得以改变。尽管如此,推动疫苗接种工作仍面临多种困难。我国自2021年5月下旬开始,已数次出现100例以上本土病例,疫情防控压力仍然巨大,迫切须在做好防护措施的同时加快疫苗接种。本文主要针对新冠疫情与接种疫苗、病毒变异的关联性,接种疫苗存在的问题及其应对措施进行综述,期望为疫苗接种在防控新冠疫情方面发挥的作用提供数据支持。
① 数据来源于https://covid19.who.int/table。
1 新冠疫苗接种情况与疫情形势新冠疫情发生后多国政府、机构和企业对疫苗开发极为重视,投入巨大,整个研发、临床试验和生产过程进展迅速,2020年底多种新冠疫苗获得紧急授权而开始使用。接种疫苗的目标包括3方面:①预防感染,大幅度降低接种者感染率; ②若有突破性感染,接种者症状减轻,少有重症甚至死亡; ③大幅度降低接种者感染后再传播给他人的可能。
1.1 部分国家或地区新冠疫苗接种情况世界范围内研发和生产疫苗最迅速的国家包括中国、美国、英国等。受疫苗产地及产能、人群接种意愿、运输及接种服务能力等因素影响,不同国家/地区接种情况差异很大,表 1统计了2021年6月初部分国家/地区的新冠疫苗接种情况。
| Location | Total Doses | Doses administered per100 people | Location | Total doses | Doses administered per100 people | |
| Mainland China | 704 826 000 | 49 | Japan | 12 343 590 | 10 | |
| United States | 296 912 892 | 89 | South Korea | 8 962 721 | 17 | |
| India | 215 678 166 | 16 | Philippines | 5 180 721 | 5 | |
| Brazil | 68 919 860 | 32 | Thailand | 3 609 882 | 5 | |
| United Kingdom | 65 658 949 | 97 | Malaysia | 3 212 873 | 0 | |
| Germany | 52 779 769 | 63 | Nepal | 2 827 243 | 10 | |
| France | 37 453 873 | 55 | Chinese Hong Kong | 2 466 461 | 33 | |
| Italy | 35 817 595 | 59 | Sri Lanka | 2 117 653 | 10 | |
| Russia | 29 792 970 | 20 | Vietnam | 1 110 111 | 1 | |
| Spain | 27 607 247 | 59 | Chinese Taiwan | 698 330 | 3 | |
| Israel | 10 587 948 | 122 | Chinese Macao | 182 969 | 28 | |
| 数据来源:用数据看世界新冠疫苗接种追踪(https://ourworldindata.org/covid-vaccinations)更新时间:2021年6月4日。 Source: Our World in Data COVID-19 vaccination tracking(https://ourworldindata.org/covid-vaccinations), updated on June 4, 2021. | ||||||
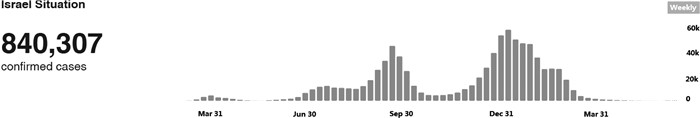
现有的新冠疫苗均是根据新冠病毒野生株研发,截至2021年10月,一些接种率较高的国家/地区疫情在短时间内得到缓解。例如,以色列在2020年12月开始接种美国辉瑞(Pfizer)与德国生物科技(BioNTech)合作研制的BNT162b2/ Comirnaty疫苗(简称辉瑞疫苗),截至2021年4月19日,全国54%的人口完成2剂疫苗接种。在接种初期该国正经历第3波疫情,最多每天新增8 328例,通过快速大规模疫苗接种后疫情得到控制,4月19日新发病例已降至每天149例,政府因此取消封城决定并放松管制措施[2]。经测算在接种第2剂疫苗7天后,预防新冠病毒野生株导致感染的有效性为95.3%[1-3]。以色列2020年3月至2021年6月的每周新增确诊病例数如图 1所示。
|
| 资料来源:世界卫生组织网站(https://covid19.who.int/table),更新时间:2021年6月24日。 Source: World Health Organization(https://covid19.who.int/table), updated on June 24, 2021. 图 1 以色列每周新增确诊病例数(2020年3月—2021年3月) Fig. 1 Weekly new confirmed cases in Israel(March 2020-March 2021) |
通过接种新冠疫苗,以色列2021年6月初每日新增病例数在20例左右,其中一半来自国外入境人员。但7月该国再次暴发疫情,可能原因包括疫苗引发的免疫力已显著降低,新冠病毒Delta变异株极高的传染性及其对疫苗存在免疫逃逸情况,防控措施放松以及儿童等人群未接种疫苗等[4]。
1.3 低接种率国家疫情加剧世界卫生组织(World Health Organization,WHO)公布的每周新增新冠确诊病例数据显示①,无论发达国家还是发展中国家,若新冠疫苗接种率低,且政府或民众防护体系存在漏洞,可能无法避免新冠疫情的加剧。
① 数据来源于https://covid19.who.int/table。
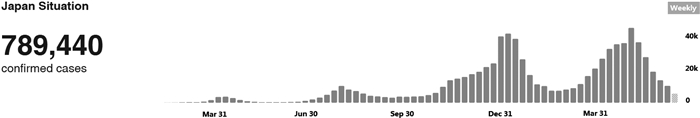
作为发达国家,日本的社会治理及公共卫生体系较完善,但入境检疫及其他防疫措施宽松,新冠疫苗接种率较低(截至5月31日,完成两剂接种者占人口比例仅为3.19%②),没能通过大面积接种疫苗来减缓疫情[5]。2020年3月到2021年6月的新冠疫情情况如图 2所示。
② 数据来源于https://ourworldindata.org/covid-vaccinations。
|
| 资料来源:世界卫生组织网站(https://covid19.who.int/table),更新时间:2021年6月24日。 Source: World Health Organization(https://covid19.who.int/table), updated on June 24, 2021. 图 2 日本每周新增确诊病例数(2020年3月-2021年3月) Fig. 2 Weekly new confirmed cases in Japan(March 2020-March 2021) |
作为发展中国家,斯里兰卡疫苗接种率低、医疗体系相对薄弱,受印度疫情波及、变异病毒传播性增强等影响,2021年5月份新冠病例数大幅度增长。2020年3月到2021年6月的新冠疫情情况见图 3。

|
| 资料来源:世界卫生组织网站(https://covid19.who.int/table),更新时间:2021年6月24日。 Source: World Health Organization(https://covid19.who.int/table), updated on June 24, 2021. 图 3 斯里兰卡每周新增确诊病例数(2020年3月-2021年3月) Fig. 3 Weekly new confirmed cases in Sri Lanka(March 2020-March 2021) |
新冠病毒作为一种核糖核酸(ribonucleic acid,RNA)病毒,易发生变异,通过基因测序可以确定病毒变异情况。不受控制的疫情,病毒传播越广泛,出现变异的可能性就越高。病毒无国界,新的病毒变异株可在全球任何地方出现,也可传播到任何地方[6]。
WHO对一些病毒变异株进行了分类和命名。截至2021年10月22日,WHO将需要全球公共卫生关注的4种变异毒株,确定为关切变异株(variants of concern, VOC),分别是最早在英国发现的B.1.1.7、在南非发现的B.1.351、在巴西发现的P.1和在印度发现的B.1.6172,对应的WHO命名的名称依次是Alpha、Beta、Gamma和Delta[7]。VOC的传染性增强,有些毒力增强,可能会降低疫苗的免疫作用。目前WHO将可导致聚集性疫情的2种病毒变异株确定为关注变异株(variants of interest, VOI),给出的名称分别是Lambda和Mu[7]。
病毒变异株在取代野生株的过程中,会因主导变异株特性差异而导致疫情发生较大变化。例如:Alpha变异株比野生株的传染性高出很多,Delta变异株比Alpha变异株传染性再高60%[8]; Delta变异株可在接种率低的国家或地区快速传播,导致大量感染、住院和死亡。2021年8月,在全球流行的新冠病毒株中,Delta变异株占比最高,在其成为主导株后,受影响的国家/地区的疫情加重[8]。我国也未能幸免,2021年7月在南京暴发并传播至扬州、张家界等地的新冠疫情比较严重,基因测序结果显示是由Delta变异株引发[9]。新冠病毒只要还在全球范围内广泛传播,就可能出现新的变异株,导致疫情局面发生改变。
1.5 疫苗接种对变异病毒的效果接种现有新冠疫苗对目前流行的多种病毒变异株显示有效。研究显示,仅接种1剂新冠(辉瑞或阿斯利康)疫苗时,对感染Alpha变异株人群的有效性接近48.7%,对感染Delta变异株人群的有效性接近30.7%;接种2剂辉瑞疫苗后,对感染Alpha、Delta变异株人群的有效性分别为93.7%和88.0%;接种2剂阿斯利康疫苗,对感染Alpha、Delta变异株人群的有效性分别是74.5%和67.0%[10]。此外,现有疫苗可大幅减少严重症状、住院和死亡数,完成2剂疫苗接种可以取得更好的保护效果[8, 10]。
2021年5月在广州暴发了由Delta变异株引发的新冠疫情,经过研究接种我国研制的灭活新冠疫苗者的感染情况,发现接种过1剂者的疫苗有效性为13.8%,达不到保护作用; 接种过2剂者疫苗有效性达到59.0%,说明疫苗具备保护作用[11]。目前多个国家针对现有疫苗对变异病毒的有效性进行评估,并研发新疫苗和改进现有疫苗,以更好地应对变异病毒[12-13]。
2 接种疫苗存在的问题及其应对措施 2.1 疫苗缺乏有很多国家由于不生产疫苗,从其他途径获得的疫苗有限,造成疫苗接种率低。截至2021年8月9日,全世界已接种44.6亿剂疫苗,其中低收入国家接种数仅为0.126亿剂[14]。若不能持续做好新冠防控工作,疫苗接种率低容易导致疫情暴发及蔓延,甚至拖累全球抗击疫情的步伐[15]。
由联合国支持的“新冠肺炎疫苗实施计划”(COVID-19 Vaccine Global Access,COVAX),其目标是让全世界没有能力自己研发和生产疫苗的国家也能及时获得新冠疫苗[16]。疫苗进入WHO紧急使用清单,要通过COVAX供应疫苗和国际采购的先决条件。截至2021年6月1日,进入WHO紧急使用清单的疫苗,包括由美国辉瑞(Pfizer)与德国生物科技(BioNTech)合作研制的疫苗、英国阿斯利康(AstraZeneca)研制的疫苗、印度血清研究所(Serum Institute of India Pvt. Ltd)研制的疫苗、美国强生公司(Janssen-Cilag International NV)研制的疫苗、美国莫德纳(Moderna)研制的疫苗,以及我国北京生物制品研究所和北京科兴中维生物技术公司研发的疫苗[17]。为了解决疫苗供应不足的问题,除了加大现有疫苗产能和合理分配外,还须研发和生产更多、更有效的疫苗[18]。
2.2 疫苗犹豫在疫苗供应充足时,可能发生疫苗犹豫的情况,即在可以接种的情况下,推迟或拒绝接种安全疫苗。疫苗犹豫受多种因素的影响,包括对疫苗安全性或有效性的顾虑、错误认知感染后果、听信虚假信息等。
2021年美国对新冠疫苗接种犹豫的一项全国快速评估报告数据显示,“极有可能”愿意接种人群占比仅为52%[19]。若疫苗犹豫的人员过多,就较难通过接种而达到群体免疫甚至影响疫情防控。各国公共卫生机构等应通过各种方式进行公众健康宣传教育,以便让公众打消顾虑,提升疫苗接种率。
2.2.1 对疫苗安全性顾虑疫苗安全性是一些疫苗犹豫者的最大顾虑,他们担心接种疫苗后可能会有各种各样的不良反应。实际上与其他疫苗一样,在接种新冠疫苗后身体会出现一些免疫反应。通常多数人没有症状,少数人出现局部或全身症状,绝大多数反应无需特殊处理,2~3天后可自行恢复。中国疾病预防控制中心发布的我国新冠疫苗接种不良反应监测情况指出,2020年12月15日—2021年4月30日, 31个省、自治区、直辖市以及新疆生产建设兵团报告接种新冠病毒疫苗2.65亿剂次,报告预防接种不良反应31 434例,报告发生率为11.86/10万剂次,其中一般反应占比高于80%,异常反应最多的依次为过敏性皮疹、血管性水肿和急性严重过敏反应[20]。
2.2.2 对疫苗有效性顾虑有些疫苗犹豫者认为,疫苗通常需要5~6年才能研制成功,而新冠疫苗的研发不到一年,因此对其有效性存在顾虑。疫苗是应对新冠疫情的重要手段,新冠疫情后多方投入大量资源进行疫苗研发等,因而在短时期内取得成功,临床试验和实际应用情况均说明疫苗效果显著。例如,在对辉瑞疫苗进行3期临床试验期间,21 720人接种疫苗,同时21 728人接种安慰剂。在完成2剂接种后,疫苗组人群中有8人感染新冠,安慰剂组人群中有162人感染新冠,因此该疫苗预防感染的有效性为95%[21]。同样进行的试验中,15 210人接种mRNA-1273疫苗,另有15 210人接种安慰剂。在完成2剂接种后,疫苗组人群中有11人感染新冠,安慰剂组人群中有185人感染,因此该疫苗预防感染的有效性为94.1%[22]。2021年2月2日—5月1日,智利对北京科兴中维生物技术公司研发疫苗进行了研究,该疫苗预防感染新冠的有效性为65.9%,预防住院的有效性为87.5%,预防进入重症监护室的有效性为90.3%,预防与新冠相关死亡的有效性为86.3%[23]。
另有研究说明在接种新冠疫苗后可以大幅度减少接种者感染、重症或死亡及传播的可能。例如,在2021年2月—4月,对入境卡塔尔国际机场旅客进行了新冠病毒核酸检测。其中,31?偋c190名旅客完成了2剂新冠疫苗接种,215 901名旅客未接种过疫苗或感染过新冠病毒,2种人群检测阳性率分别是0.82%和3.74%,说明接种疫苗可使感染率降低[24]。以色列全国性接种数据显示,已接种2剂疫苗者比没有接种者在减少严重疾病及死亡方面,分别有97.5%及96.7%的效果[1]。还有研究显示,已完成疫苗接种者感染时,其传染给家人的可能性比未接种者低78.6%[25]; 另有对36.5万英国家庭的研究显示,接种过1剂疫苗者将新冠病毒传给家人的可能性比未接种者少40%~50%[26]。
2.2.3 错误认知感染后果仍有相当部分人群对感染新冠的风险认识严重不足,错误地认为自己感染可能性低,即使感染也症状轻微、不必重视,或由于种种偏见而认为接种疫苗风险更高。应告知这类人群感染新冠的严重后果,以便知晓接种疫苗利大于弊。由于新冠病毒易变异,疫情在不断变化,一些变异株使得老年人、青年人和儿童等各年龄段都可能被感染,症状加重甚至死亡。例如,印度在2021年5月多日新增确诊病例在40万以上,且集中出现大量死亡病例,后果严重。除了急性期发作外,约10%的患者在新冠肺炎后经历长久患病[27-28]。武汉三家医院观察了1 733名新冠肺炎痊愈患者在出院6个月内的后遗症:感觉疲劳乏力的占63%、报告失眠的占26%、焦虑和抑郁的占23%、肾功能异常的占13%,有些重症患者在出院6个月后肺功能仍未恢复[29]。
2.2.4 听信虚假信息关于疫苗的虚假信息有可能传播得更快,科学常识掌握少的人群更易轻信传闻。官方机构应正面应对虚假信息,加大宣传,及时传递关于新冠的准确信息,包括疫苗的研发、临床试验、安全性、有效性等,告知接种能保护自己和家人等。医务工作者也可经常宣讲科学知识,以便打消一些人的接种顾虑[30-31]。
2.3 疫苗难以运输储存有些新冠疫苗因为制造工艺特点,对运输和储存有比较苛刻的要求。例如,辉瑞疫苗需要-70 ℃以下的储存运输条件,莫德纳疫苗也须在-20℃以下储存运输。很多国家难以符合特殊运输储存条件,还面临接种服务基础设施不足等问题。我国已获WHO批准的两款疫苗均可在2~8℃条件下储存运输,适用于基础设施条件一般的国家。此外,多国仍在不断研发新的疫苗、改进现有的疫苗,以便适合运输和储存。
3 有效的疫情防控措施 3.1 进一步加快疫苗接种加快疫苗接种可显著降低感染、住院及死亡病例数。有研究显示,若变异株传染性比野生株高30%,在每天疫苗接种量从100万增加到300万剂次时,300天内将避免152 048例住院及48 448例死亡[6]。
多个关注和关切病毒变异株的出现,对接种疫苗的速度提出更高的需求。当人群通过接种疫苗或自然感染某疾病而达到群体免疫阈值时,可有效防止该病的传播。群体免疫阈值与基本再生数R0相关,简单的模型是假设疫苗有效性为100%,且可终生保护,群体免疫阈值等于1-1/R0(例如,当R0=4时,对应的群体免疫阈值为75%)。新冠病毒在刚开始传播期间多数国家R0在2.5~3.5,但变异株传播力较野生株强,R0升高,(例如,Delta变异株的R0在5~8);在R0为6时,疫苗接种率须在83.3%以上才能达到群体免疫[8, 32]。
我国首先对18岁以上人群开展新冠疫苗接种,其次是12~17岁儿童,然后3~11岁儿童。截至2021年9月18日,我国完成2针全程接种的人员占比71%,仅接种1针的人员占比为5.4%①。
① 数据来源于https://ourworldindata.org/covid-vaccinations。
截至10月28日,全程接种率高于71%的国家有阿拉伯联合酋长国(86%)、西班牙(80%)、智利(76%)和乌拉圭(75%)[33]。
由于婴幼儿也是易感人群,可能感染新冠,且目前新冠疫苗接种还未扩大至3岁以下年龄组,故成年人及3岁以上儿童更高的疫苗覆盖率,可间接保护婴幼儿。对于有婴幼儿的家庭成员更应尽快接种。
3.2 做好各类防控措施对于全程免疫为2针剂的新冠疫苗来说,通常在接种第2剂疫苗一段时间后,才能产生期望的保护作用,由于不能达到100%的保护且免疫力随着时间推移可能降低等,接种后仍须做好戴口罩、勤洗手、保持社交距离等各种个人防护措施。在群体免疫屏障建成前,政府部门应根据实际情况,实施包括检疫隔离、密接追踪、核酸筛查、规范集会等各种强有力的防控措施[34]。
3.3 疫苗加强接种由Delta变异株主导的新一轮新冠疫情在加剧世界范围内公共卫生危机的同时,引发了对已接种人群进行疫苗加强接种的思考。一项对辉瑞疫苗接种后的回顾性研究显示,该疫苗对预防Delta变异株导致感染的有效性,在完成全程接种后的第1个月是93%,4个月后降到53%;对其他变异株的有效性在完成全程接种后的第1个月是97%,4~5个月后降到67%。说明疫苗有效性可能会在接种几个月后下降,需要通过加强接种来恢复免疫力[35-36]。
有些国家进行了疫苗加强接种的实践,例如以色列在2021年7月底开始对完成基础免疫的部分人群进行加强接种。对110万以上人群的研究显示,加强接种者比没有加强接种者的新冠感染率下降了89.69%,重症率下降了92.80%[4]。
WHO于2021年10月4日发布了关于新冠疫苗加强接种的临时声明,认为在疫苗有效性不充分时,可实施加强接种。加强接种的需要程度取决于疫苗产品的类别、目标人群、正在流行的新冠病毒(特别是关注变异株)以及暴露情况。由于世界范围内新冠疫苗供应不足,WHO认为疫苗应优先保证更多人完成基础免疫[37]。
我国多个省市已从11月份开始,全面启动对重点人群的新冠疫苗加强接种。有研究显示,对已接种2针科兴疫苗者6~8个月后进行加强接种时,抗体水平显著提高,说明加强接种可大幅提升对新冠病毒的免疫力[38]。
由于新冠疫情在持续变化、病毒变异株的出现、接种后一段时间免疫力降低等,目前无法根据所掌握的数据,来确定包括时间间隔及次数在内的完整加强接种方案[39]。
虽然持续做好个人防护也能预防新冠,但若人们无法获得免疫力,属于易感人群,始终存在感染病毒的可能。目前还存在一些未知因素,但接种疫苗仍然是控制新冠肺炎疫情并使生活恢复常态的唯一方法。若有很多人不愿意接种疫苗,则很难达到群体免疫的目标。因此,在保持各项政府及民众疫情防护措施的同时,须加强对疫苗犹豫者的宣传教育,扩大疫苗接种范围并加快接种,才能使人类早日战胜病魔,尽快回归正常生活[8]。
| [1] |
Haas EJ, Angulo FJ, McLaughlin JM, Anis E, Singer SR, Khan F, Brooks N, Smaja M, Pan K, Southern J, Swerdlow DL, Jodar L, Levy Y, Preis SA. Impact and effectiveness of mRNA BNT162b2 vaccine against SARS-CoV-2 infections and COVID-19 cases, hospitalisations, and deaths following a nationwide vaccination campaign in Israel: an observational study using national surveillance data[J]. Lancet, 2021, 397(10287): 1819-1829.
[DOI]
|
| [2] |
Leshem E, Wilder-Smith A. COVID-19 vaccine impact in Israel and a way out of the pandemic[J]. Lancet, 2021, 397(10287): 1783-1785.
[DOI]
|
| [3] |
Lustig Y, Zuckerman N, Nemet I, Atari N, Kliker L, Regev-Yochay G, Sapir E, Mor O, Alroy-Preis S, Mendelson E, Mandelboim M. Neutralising capacity against Delta (B.1.617.2) and other variants of concern following Comirnaty (BNT162b2, BioNTech/Pfizer) vaccination in health care workers, Israel[J]. Euro Surveill, 2021, 26(26): 2100557.
[DOI]
|
| [4] |
Bar-On YM, Goldberg Y, Mandel M, Bodenheimer O, Freedman L, Kalkstein N, Mizrahi B, Alroy-Preis S, Ash N, Milo R, Huppert A. Protection of BNT162b2 vaccine booster against Covid-19 in Israel[J]. N Engl J Med, 2021, 385(15): 1393-1400.
[DOI]
|
| [5] |
Kosaka M, Hashimoto T, Ozaki A, Tanimoto T, Kami M. Delayed COVID-19 vaccine roll-out in Japan[J]. Lancet, 2021, 397(10292): 2334-2335.
[PubMed]
|
| [6] |
Sah P, Vilches TN, Moghadas SM, Fitzpatrick MC, Singer BH, Hotez PJ, Galvani AP. Accelerated vaccine rollout is imperative to mitigate highly transmissible COVID-19 variants[J]. E Clinical Medicine, 2021, 35: 100865.
[DOI]
|
| [7] |
World Health Organization. Tracking SARS-CoV-2 Variants[EB/OL]. (2021-10-22)[2021-10-27]. https://www.who.int/en/activities/tracking-SARS-CoV-2-variants.
|
| [8] |
Del Rio C, Malani PN, Omer SB. Confronting the delta variant of SARS-CoV-2, summer 2021[J]. JAMA, 2021, 326(11): 1001-1002.
[DOI]
|
| [9] |
Liu Y, Yang B, Liu L, Jilili M, Yang A. Occupational characteristics in the outbreak of the COVID-19 delta variant in Nanjing, China: rethinking the occupational health and safety vulnerability of essential workers[J]. Int J Environ Res Public Health, 2021, 18(20): 10734.
[DOI]
|
| [10] |
Bernal JL, Andrews N, Gower C, Gallagher E, Simmons R, Thelwall S, Stowe J, Tessier E, Groves N, Dabrera G, Myers R, Campbell CNJ, Amirthalingam G, Edmunds M, Zambon M, Brown KE, Hopkins S, Chand M, Ramsay M. Effectiveness of Covid-19 vaccines against the B.1.617.2 (delta) variant[J]. N Engl J Med, 2021, 385: 585-594.
[DOI]
|
| [11] |
Li XN, Huang Y, Wang W, Jing QL, Zhang CH, Qin PZ, Guan WJ, Gan L, Li YL, Liu WH, Dong H, Miao YT, Fan SJ, Zhang ZB, Zhang DM, Zhong NS. Effectiveness of inactivated SARS-CoV-2 vaccines against the Delta variant infection in Guangzhou: a test-negative case-control real-world study[J]. Emerg Microbes Infect, 2021, 10(1): 1751-1759.
[DOI]
|
| [12] |
Mallapaty S. COVID vaccines slash viral spread-but Delta is an unknown[J]. Nature, 2021, 596(7870): 17-18.
[DOI]
|
| [13] |
Krause PR, Fleming TR, Longini IM, Peto R, Briand S, Heymann DL, Beral V, Snape MD, Rees H, Ropero AM, Balicer RD, Cramer JP, Muñoz-Fontela C, Gruber M, Gaspar R, Singh JA, Subbarao K, Van Kerkhove MD, Swaminathan S, Ryan MJ. Henao-Restrepo AM (2021) SARS-CoV-2 variants and vaccines[J]. N Engl J Med, 2021, 385: 179-186.
[DOI]
|
| [14] |
The Lancet. Access to COVID-19 vaccines: looking beyond COVAX[J]. Lancet, 2021, 397(10278): 941.
[DOI]
|
| [15] |
Asundi A, O'Leary C, Bhadelia N. Global COVID-19 vaccine inequity: the scope, the impact, and the challenges[J]. Cell Host Microbe, 2021, 29(7): 1036-1039.
[DOI]
|
| [16] |
World Health Organization. COVAX Working for global equitable access to COVID-19 vaccines[EB/OL]. (2022-02-28). https://www.who.int/initiatives/act-accelerator/ covax
|
| [17] |
World Health Organization. WHO validates Sinovac COVID-19 vaccine for emergency use and issue interim policy recommendations[EB/OL]. (2021-06-01)[2021-06-23]. https://www.who.int/news/item/01-06-2021-who-validates-sinovac-covid-19-vaccine-for-emergency-use-and-issues-interim-policy-recommendations.
|
| [18] |
Wouters OJ, Shadlen KC, Salcher-Konrad M. Challenges in ensuring global access to COVID-19 vaccines: production, affordability, allocation, and deployment[J]. Lancet, 2021, 397: 1023-34.
[DOI]
|
| [19] |
Khubchandani J, Sharma S, Price JH, Michael JW, Wiblishauser MJ, Sharma M, Webb FJ. COVID-19 vaccination hesitancy in the United States: a rapid national assessment[J]. J Community Health, 2021, 46(2): 270-277.
[DOI]
|
| [20] |
中国疾病预防控制中心. 全国新冠病毒疫苗预防接种不良反应监测信息概况[EB/OL]. (2021-05-28)[2021-10-30]. https://www.chinacdc.cn/jkzt/ymyjz/ymyjjz_6758/ 202105/t20210528_230911.html.
|
| [21] |
Polack FP, Thomas SJ, Kitchin N, Fernando P., Polack M. D, Thomas SJ, Kitchin N, Absalon J, Gurtman A, Lockhart S, Perez JL, Marc GP, Moreira ED, Zerbini C, Bailey R, Swanson KA, Roychoudhury S, Koury K, Li P, Kalina WV, Cooper D, Frenck RW, Hammitt LL, Türeci Ö, Nell H, Schaefer A, Ünal S, Tresnan DB, Mather S, Dormitzer PR, ahin S, Jansen KU, Gruber WC. Safety and efficacy of the BNT162b2 mRNA Covid-19 vaccine[J]. N Engl J Med, 2020, 383(27): 2603-2615.
[DOI]
|
| [22] |
Baden LR, Sahly HME, Essink B, Kotloff K, Frey S, Novak R, Diemert D, Spector SA, Rouphael N, Creech CB, McGettigan J, Khetan S, Segall N, Solis J, Brosz A, Fierro C, Schwartz H, Neuzil K, Corey L, Gilbert P, Janes H, Follmann D, Marovich M, Mascola J, Polakowski L, Ledgerwood J, Graham BS, Bennett H, Pajon R, Knightly C, Leav B, Deng WP, Zhou HH, Han S, Ivarsson M, Miller J, Zaks T. Efficacy and safety of the mRNA-1273 SARS-CoV-2 vaccine[J]. N Engl J Med, 2021, 384: 403-416.
[DOI]
|
| [23] |
Jara A, Undurraga EA, González C, Paredes F, Fontecilla T, Jara G, Pizarro A, Acevedo J, Leo K, Leon F, Sans C, Leighton P, Suárez P, García-Escorza H, Araos R. Effectiveness of an inactivated SARS-CoV-2 vaccine in Chile[J]. N Engl J Med, 2021, 385(10): 875-884.
[DOI]
|
| [24] |
Bertollini R, Chemaitelly H, Yassine HM, Al-Thani MH, Al-Khal A, Abu-Raddad LJ. Associations of vaccination and of prior infection with positive PCR test results for SARS-CoV-2 in airline passengers arriving in Qatar[J]. JAMA, 2021, 326(2): 185-188.
[DOI]
|
| [25] |
Prunas O, Warren JL, Crawford FW, Gazit S, Patalon T, Weinberger DM, Pitzer VE. Vaccination with BNT162b2 reduces transmission of SARS-CoV-2 to household contacts in Israel[OL]. medRxiv. doi: 10.1101/2021.07.13.21260393.
|
| [26] |
Harris RJ, Hall JA, Zaidi A, Andrews NJ, Dunbar JK, Dabrera G. Effect of vaccination on household transmission of SARS-CoV-2 in England[OL]. N Engl J Med, 2021, 385: 759-760.
|
| [27] |
Kuppalli K, Gala P, Cherabuddi K, Kalantri SP, Mohanan M, Mukherjee B, Pinto L, Prakash M, Pramesh CS, Rathi S, Pai NP, Yamey G, Pai M. India's COVID-19 crisis: a call for international action[J]. Lancet, 2021, 397(10290): 2132-2135.
[DOI]
|
| [28] |
Greenhalgh T, Knight M, A'Court C, Buxton M, Husain L. Management of post-acute covid-19 in primary care[J]. BMJ, 2020, 370: m3026.
[DOI]
|
| [29] |
Huang CL, Huang LX, Wang YM, Li X, Ren LL, Gu XY, Kang L, Guo L, Liu M, Zhou X, Luo JF, Huang ZH, Tu SJ, Zhao Y, Chen L, Xu DC, Li YP, Li CH, Peng L, Li Y, Xie WX, Cui D, Shang LH, Fan GH, Xu JY, Wang G, Wang Y, Zhang JC, Wang C, Wang JW, Zhang DY, Cao B. 6-month consequences of COVID-19 in patients discharged from hospital: a cohort study[J]. Lancet, 2021, 397(10270): 220-232.
[DOI]
|
| [30] |
Steffens MS, Dunn AG, Wiley KE, Leask J. How organizations promoting vaccination respond to misinformation on social media: a qualitative investigation[J]. BMC Public Health, 2019, 19(1): 1348.
[DOI]
|
| [31] |
SteelFisher GK, Blendon RJ, Caporello H. Encouraging acceptance of Covid-19 vaccines[J]. N Engl J Med, 2021, 384: 1483-1487.
[DOI]
|
| [32] |
Anderson RM, Vegvari C, Truscott J, Collyer BS. Challenges in creating herd immunity to SARS-CoV-2 infection by mass vaccination[J]. Lancet, 2020, 396(10263): 1614-1616.
[DOI]
|
| [33] |
Our world in Data. Coronavirus (COVID-19) Vaccinations[EB/OL]. [2021-10-30]. https://ourworldindata.org/covid-vaccinations.
|
| [34] |
Giordano G, Colaneri M, Di Filippo A, Blanchini F, Bolzern P, Nicolao GD, Sacchi P, Colaneri P, Bruno R. Modeling vaccination rollouts, SARS-CoV-2 variants and the requirement for non-pharmaceutical interventions in Italy[J]. Nat Med, 2021, 27(6): 993-998.
[DOI]
|
| [35] |
Callaway E. COVID vaccine boosters: the most important questions[J]. Nature, 2021, 596: 178-180.
[DOI]
|
| [36] |
Tartof SY, Slezak JM, Fischer H, Hong V, Ackerson BK, Ranasinghe ON, Frankland TB, Ogun OA, Zamparo JM, Gray S, Valluri SR, Pan K, Angulo FJ, Jodar L, McLaughlin JM. Effectiveness of mRNA BNT162b2 COVID-19 vaccine up to 6 months in a large integrated health system in the USA: a retrospective cohort study[J]. Lancet, 2021, 398(10309): 1407-1416.
[DOI]
|
| [37] |
World Health Organization. Interim statement on booster doses for COVID-19 vaccination[EB/OL]. (2021-10-04)[2021-10-30]. https://www.who.int/news/item/04-10-2021-interim-statement-on-booster-doses-for-covid-19-vaccination.
|
| [38] |
Pan HX, Wu QH, Zeng G, Yang J, Deng XW, Chu K, Zheng W, Zhu FC, Yu HJ, Yin WD. Immunogenicity and safety of a third dose, and immune persistence of CoronaVac vaccine in healthy adults aged 18-59 years: interim results from a double-blind, randomized, placebo-controlled phase 2 clinical trial[EB/OL]. medRxiv, 2021. doi: 10.1101/2021.07.23.21261026.
|
| [39] |
Kherabi Y, Fiolet T, Rozencwajg S, Salaün JP, Peiffer-Smadja N. COVID-19 vaccine boosters: what do we know so far?[J]. Anaesth Crit Care Pain Med, 2021, 40(6): 100959.
[DOI]
|
 2021, Vol. 16
2021, Vol. 16


