肺炎支原体(Mycoplasma pneumoniae)是一种介于细菌与病毒、能独立生长繁殖的最小原核细胞型微生物,可引起上呼吸道感染、支气管炎、肺炎等疾病,其中肺炎支原体肺炎(Mycoplasma pneumoniae pneumonia,MPP)占儿童社区获得性肺炎(community-acquired pneumonia,CAP)的10%~40%[1]。近年来,MPP导致的免疫损伤机制备受关注。机体感染肺炎支原体后免疫力低下,易合并细菌或病毒感染,其中Epstein-Barr病毒(Epstein-Barr virus,EBV)是常见病原体之一。临床发现,MPP合并EBV感染较单纯MPP引起的肺内及肺外损伤更严重,多数观点认为主要与细胞免疫机制有关[2-3]。本研究拟通过检测MPP合并EBV感染患儿血清中白细胞介素6(interleukin 6,IL-6)、IL-4、γ干扰素(interferon γ,IFN-γ)、IL-10的水平变化,了解患儿机体免疫状态,探讨这些指标在MPP合并EBV感染诊断中的临床应用价值。
1 材料与方法 1.1 研究对象选取2016年9月—2017年3月上海市第六人民医院儿科住院部收治的MPP合并EBV感染患儿作为观察组(A组),单纯MPP患儿作为单纯感染对照组(B组),小儿骨科择期行六指切除手术患儿(近期无感染)作为健康对照组(C组)。A组61例,B组103例,C组23例。根据2013年中华医学会儿科学分会呼吸学组修订的儿童重症肺炎诊断标准[4],将A组患儿分为重症肺炎组和普通肺炎组,其中重症肺炎组15例,普通肺炎组46例。
1.2 纳入及排除标准MPP诊断标准[5]:①符合第8版《诸福棠实用儿科学》支原体肺炎临床特点;②单份血清肺炎支原体特异性IgM抗体效价≥1:160,或短期(1周)内双份血清肺炎支原体IgM抗体效价上升4倍及以上,或短期(1周)内双份血清肺炎支原体IgM抗体效价阴性转阳性。
EBV感染诊断标准[6-7]:①EBV衣壳抗原(viral capsid antigen,VCA)IgM(+)或早期抗原(early antigen,EA)IgG(+),且抗EBV核抗原(EBV nuclear antigen,EBNA)IgG (-)。
重症肺炎诊断标准[4]:符合2013年中华医学会儿科学分会呼吸学组制定的儿童重度社区获得性肺炎(community-acquired pneumonia,CAP)诊断标准,存在以下任何一项:①一般情况差;②拒食或脱水征;③有意识障碍;④呼吸频率明显增快(婴儿>70次/min,年长儿>50次/min);⑤发绀;⑥呼吸困难(呻吟、鼻翼翕动、三凹征);⑦多肺叶或≥2/3的肺受累;⑧胸腔积液;⑨脉搏血氧饱和度≤0.92;⑩肺外并发症。
排除标准:①病程中出现呼吸道以外的感染症状,包括皮肤、泌尿系统感染等;②长期使用糖皮质激素或近3个月内使用免疫球蛋白等免疫抑制剂和免疫调节剂。
1.3 实验方法所有患儿均于入院第2天采集静脉血。采用被动凝集法检测肺炎支原体特异性IgM抗体,试剂盒购自富士瑞必欧株式会社。采用德国欧蒙公司酶联免疫吸附试验(enzyme-linked immunosorbent assay,ELISA)试剂盒检测EBV特异性抗体,按说明书操作。留取静脉血2.0 mL,自然凝固10~20 min,3 000 r/min离心20 min,取血清,-80 ℃保存。用酶标仪测光密度(optical density,OD)。
本研究获得所有患儿监护人的知情同意,并经上海市第六人民医院医学伦理委员会批准。
1.4 统计学方法采用SPSS 18.0软件进行统计学分析。所有数据以x±s表示,并进行正态性及方差齐性检验,3组之间比较采用单因素方差分析,两组之间比较采用独立样本t检验,P<0.05为差异有统计学意义。
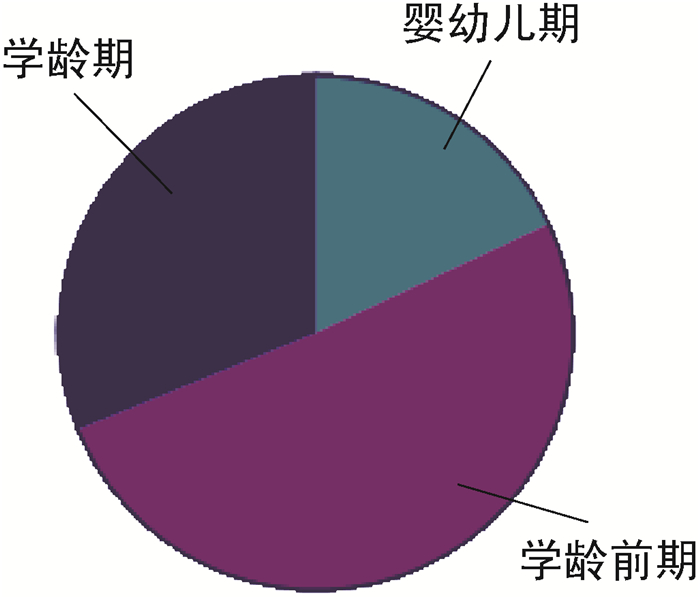
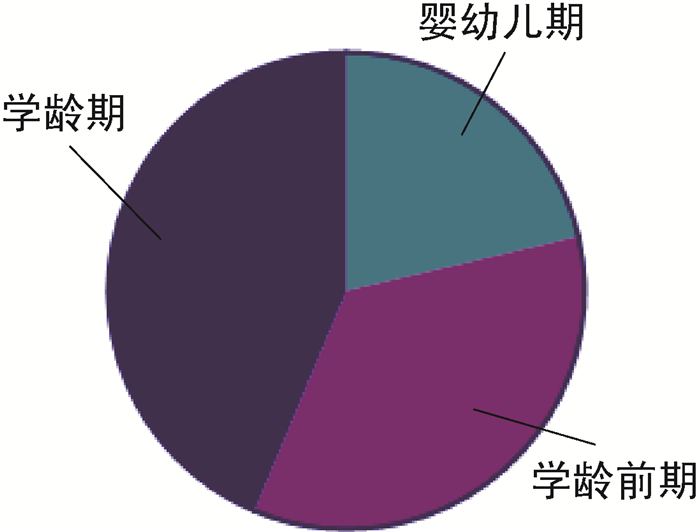
2 结果 2.1 一般资料A组患儿中,男33例,女28例,平均年龄(5.24±1.38)岁;其中婴幼儿期11例(18.03%),学龄前期31例(50.82%),学龄期19例(31.14%)。B组患儿中,男65例,女38例,平均年龄(4.01±3.25)岁;其中婴幼儿期22例(21.36%),学龄前期36例(34.95%),学龄期45例(43.69%)。C组患儿中,男15例,女8例,平均年龄(6.31±0.65)岁;其中婴幼儿期2例(8.70%),学龄前期5例(21.74%),学龄期16例(69.57%)。3组患儿的年龄分布及性别差异均无统计学意义(图 1~2)。
|
| 图 1 MPP合并EBV感染患儿的年龄分布 Fig. 1 Distribution of age in children with MPP combined with EBV infection |
|
| 图 2 单纯MPP患儿的年龄分布 Fig. 2 Distribution of age in children with MPP |
3组患儿血清IL-6、IL-4、IFN-γ、IL-10水平差异显著。其中A和B组IL-6、IL-4、IFN-γ、IL-10水平高于C组(P<0.05),A组IL-6、IL-10水平高于B组(P<0.05),而A与B组IFN-γ、IL-4水平差异无统计学意义(表 1)。
| Group | n | IL-6 | IL-4 | IFN-γ | IL-10 |
| A | 61 | 68.00±9.17*# | 13.80±1.06* | 40.71±1.88* | 25.50±1.71*# |
| B | 103 | 35.00±7.46* | 10.91±2.84* | 40.50±10.42* | 15.52±6.03* |
| C | 23 | 12.51±0.46 | 7.93±2.65 | 14.71±1.88 | 5.52±1.03 |
| F value | 5.734 | 1.548 | 0.768 | 7.352 | |
| P value | 0.034 | 1.87 | 0.923 | 0.001 | |
| *P<0.05 compared with group C, #P<0.05 compared with group B. | |||||
A组重症组患儿血清IL-6、IL-10、IL-4水平高于非重症组(P<0.05),而IFN-γ水平无统计学差异(表 2)。
| Group | n | IL-6 | IL-4 | IFN-γ | IL-10 |
| Severe | 15 | 67.00±2.17* | 28.83±2.46* | 35.71±3.52 | 24.47±2.86* |
| Non-severe | 46 | 49.67±8.46 | 14.91±6.34 | 35.82±11.43 | 13.56±10.49 |
| F value | 11.331 | 5.769 | 14.238 | 5.492 | |
| P value | 0.000 | 0.049 | 1.096 | 0.000 | |
| *P<0.05. | |||||
MPP最常见的临床表现有发热、咳嗽及喘息。由于肺炎支原体与心、脑、肺、肝及平滑肌等多种人体组织器官存在部分相同抗原,其感染后除引起肺部炎症外,还累及血液、皮肤、消化、心血管、中枢神经等引起多系统损伤。MPP的临床症状轻重程度不一,严重者可危及生命。关于MPP的发病机制,国内外学者主要倾向以下两种。①黏附损伤:肺炎支原体借助黏附素吸附于宿主细胞后,产生过氧化氢、超氧化基团和神经毒素等,引起呼吸道上皮细胞的氧化应激反应,并分泌社区获得性呼吸窘迫综合征(community-acquired respiratory distress syndrome,CARDS)毒素等,对呼吸道上皮造成损伤。②免疫损伤:包括自身免疫损伤和免疫抑制损伤。自身免疫损伤即肺炎支原体感染后产生的抗肺、脑及其他组织的自身抗体与抗原结合形成抗原-抗体免疫复合物,补体和免疫细胞在自身抗体和免疫复合物的诱导下被激活,从而削弱机体免疫屏障。免疫抑制损伤即肺炎支原体侵入宿主后破坏正常T细胞与B细胞比例,造成淋巴细胞多克隆活化,破坏CD4+/CD8+动态平衡,使Th1/Th2失衡,引起机体免疫抑制。EBV是一种嗜B细胞疱疹病毒,在儿科病毒感染性疾病中非常普遍。病毒携带者和病毒感染者是传染源,主要通过亲吻等经口密切接触的行为传播,因此被称为“接吻病毒”。由于传染源广泛、传播途径简单,EBV初发感染多发生于儿童时期,90%以上学龄前儿童曾感染过EBV[8]。EBV首先侵犯上皮细胞和B细胞,通过gp350/200与B细胞表面的CR2结合而进入B细胞,并诱导其分化为记忆性B细胞,形成长期潜伏感染,在宿主免疫力低下或环境改变时EBV大量激活,引起疾病[9]。EBV感染可使多器官、多系统受累,首发症状不一。6岁以下儿童原发性EBV感染大多表现为无症状感染或上呼吸道感染等非特异性表现;但在青少年期,约50%的原发性EBV感染可表现为传染性单核细胞增多症[10-11]。
近年来国内大量研究发现,MPP合并EBV感染患儿较单纯MPP患儿的肺内外炎症更严重,疾病更多样化。这可能与肺炎支原体和EBV的免疫机制相似有关,均表现为T细胞亚群紊乱,即CD4+/CD8+比例失调[12]。肺炎支原体感染可引起CD4+ T细胞凋亡,导致细胞免疫功能下降,进而激活长期潜伏于体内的EBV侵入B细胞,致使B细胞变性、凋亡,同时引起T细胞的强烈反应,CD8+T细胞大量增殖,免疫反应叠加,导致组织损伤加重[13-14]。IL-6、IL-4、IFN-γ、IL-10是重要的免疫细胞因子,在细胞免疫评价方面有重要作用。
Th细胞按功能分为Thl及Th2亚群。Th1通过分泌IL-2、IFN-γ、IL-12等促炎细胞因子介导细胞免疫应答,增强杀伤炎症细胞的细胞毒性作用;Th2通过分泌IL-4、IL-10、IL-5等抗炎细胞因子促进B细胞产生抗体,主要参与体液免疫调节。正常情况下,Th1/Th2比值处于动态平衡,一旦病理因素涉入,两者比值失衡,即导致机体出现相应的病理损伤。
刘文彬等[15]认为,肺炎衣原体感染可抑制Th细胞产生IL-2,从而使细胞免疫功能低下,易合并病毒感染或使原有病毒激活。低剂量IL-2可阻止EBV介导的淋巴组织增生性疾病[16]。有研究发现[17],IL-2通过IL-6发挥免疫效应,而IL-6间接抑制细胞免疫功能。IL-6主要由活化的T细胞和B细胞、单核-巨噬细胞、内皮细胞等生成,可诱导B细胞分化并产生免疫球蛋白,促进T细胞增殖生长,具有免疫调节、促炎和抗感染等生物学作用[18-19]。当机体处于炎症和感染状态时,IL-6可促进CD4+ T细胞在Th2分化期间的IL-4产生,配合转化生长因子p(transforming growth factor p,TGF-p)抑制Thl分化,阻止活化的CD4+ T细胞凋亡[20]。肺炎支原体可通过细胞酪氨酸磷酸化信号转导和核因子κB(nuclear factor κB,NF-κB)激活,诱导单核细胞产生IL-6,继而引发促炎因子级联反应,增强中性粒细胞趋化及脱颗粒黏附作用,加剧炎症反应[21-22]。本研究发现,MPP合并EBV感染和单纯MPP患儿血清IL-6水平高于健康对照患儿,且MPP合并EBV感染所致重症肺炎患儿IL-6水平高于非重症肺炎患儿,表明IL-6可反映免疫损伤程度,与Tian等[23]的研究结论一致。
IL-4是Th0分化为Th2的关键细胞因子;IFN-γ可促进Th0向Th1分化,并减少IL-4 mRNA表达,从而抑制Th2分化过程[24]。MPP患儿肺泡灌洗液中,高菌量组IL-4水平及IL-4/IFN-γ比值显著高于低菌量组,提示肺炎支原体导致的Th1/Th2免疫偏移以Th2免疫反应占优势[25-26]。这种改变有利于机体清除病原体,削弱肺炎支原体感染引起的炎症反应。有文献报道,肺炎支原体感染机体后,IFN-γ水平明显升高,表明Th1/Th2免疫失衡以Th1占优势[27]。本研究发现,MPP合并EBV感染患儿的IL-4、IFN-γ水平较健康对照组升高,提示MPP合并EBV感染患儿存在Th1/Th2免疫平衡失调。随着病情加重,IL-4升高更显著,且Th2细胞免疫起主导作用。MPP合并EBV感染患儿的IL-4、IFN-γ水平与单纯MPP组相比无明显差异,可能与感染不同时期有关。Li等[28]发现,MPP急性期Th1占优势,恢复期转变为以Th2为主,表明MPP合并EBV感染后细胞免疫可由Th1向Th2转变。
IL-10具有强抗炎和负向免疫调控作用,可直接拮抗IL-6、肿瘤坏死因子α(tumor necrosis factor α,TNF-α)等炎性因子的释放以减轻机体炎症反应。出现炎症瀑布反应时,IL-10主要通过抑制抗原呈递细胞(antigen presenting cell,APC),间接降低T细胞活性和免疫应答能力来抑制免疫功能,从而大大增加机体再次感染的概率[29-30]。研究证实,诱导性调节性T细胞(induced regulatory T cell,iTreg)主要通过分泌IL-10来发挥负向免疫调节作用[31],而Th17/Treg免疫平衡与MPP的发生发展密切相关[32-34]。本研究提示,MPP合并EBV感染及单纯MPP患儿血清IL-10水平显著升高,混合感染所致重症肺炎患儿血清IL-10较普通肺炎更高,原因可能是免疫抑制增加了感染概率而使病情加重。
综上所述,Th1/Th2细胞免疫功能紊乱在MPP合并EBV感染的发生发展中起重要作用。肺炎支原体、EBV可通过诱导机体分泌IL-6、IL-4、IFN-γ、IL-10造成组织损伤,这些指标对评估MPP合并EBV感染患儿的细胞免疫紊乱程度有重要意义。
| [1] |
中华医学会儿科学分会呼吸学组, 《中华实用儿科临床杂志》编辑委员会. 儿童肺炎支原体肺炎诊治专家共识(2015年版)[J]. 中华实用儿科临床杂志, 2015, 30(17): 1304-1308. [DOI]
|
| [2] |
陈斌斌. 肺炎支原体合并EB病毒感染患儿的临床特点及免疫研究[J]. 临床和实验医学杂志, 2015, 14(5): 405-408. [DOI]
|
| [3] |
Ding L, Ji W, Sun HM, Jiang WJ, Gu WJ, Yan YD, Shao XJ. Association of T lymphocyte subsets and allergens with Mycoplasma pneumoniae infection complicated by wheezing in infants and young children[J]. Zhongguo Dang Dai Er Ke Za Zhi, 2016, 18(12): 1254-1258.
[PubMed]
|
| [4] |
中华医学会儿科学分会呼吸学组, 《中华儿科杂志》编辑委员会. 儿童社区获得性肺炎管理指南(2013修订)(上)[J]. 中华儿科杂志, 2013, 51(10): 745-752. [DOI]
|
| [5] |
江载芳, 申昆玲, 沈颖. 诸福棠实用儿科学[M]. 第8版. 北京: 人民卫生出版社, 2015: 1280-1283.
|
| [6] |
王群, 谢正德. 儿童EB病毒相关疾病的诊断标准和治疗原则[J]. 中华实用儿科临床杂志, 2010, 25(10): 706-708. [URI]
|
| [7] |
De Paschale M, Clerici P. Serological diagnosis of Epstein-Barr virus infection:Problems and solutions[J]. World J Virol, 2012, 1(1): 31-43.
[DOI]
|
| [8] |
汪洋, 许红梅. EB病毒的流行病学研究进展[J]. 国际检验医学杂志, 2010, 31(12): 1405-1407. [DOI]
|
| [9] |
刘璐瑶, 孙金峤, 王晓川. EB病毒感染的免疫机制研究进展[J]. 中国循证儿科杂志, 2017, 12(3): 219-232. [DOI]
|
| [10] |
Dunmire SK, Hogquist KA, Balfour HH. Infectious mononucleosis[J]. Curr Top Microbiol Immunol, 2015, 390(Pt 1): 211-240.
[PubMed]
|
| [11] |
中华医学会儿科学分会感染学组, 全国儿童EB病毒感染协作组. 儿童主要非肿瘤性EB病毒感染相关疾病的诊断和治疗原则建议[J]. 中华儿科杂志, 2016, 54(8): 563-568. [DOI]
|
| [12] |
Hussein K, Maecker-Kolhoff B, Donnerstag F, Laenger F, Kreipe H, Jonigk D. Epstein-Barr virus-associated smooth muscle tumours after transplantation, infection with human immunodeficiency virus and congenital immunodeficiency syndromes[J]. Pathobiology, 2013, 80(6): 297-301.
[DOI]
|
| [13] |
Coleman CB, Wohlford EM, Smith NA, King CA, Ritchie JA, Baresel PC, Kimura H, Rochford R. Epstein-Barr virus type 2 latently infects T cells, inducing an atypical activation characterized by expression of lymphotactic cytokines[J]. J Virol, 2015, 89(4): 2301-2312.
[DOI]
|
| [14] |
高颖, 白涛敏, 王杰民, 焦富勇. 儿童肺炎支原体合并EB病毒感染的临床研究及免疫分析[J]. 陕西医学杂志, 2014, 43(10): 1394-1395. [DOI]
|
| [15] |
刘文彬, 赵文利, 汤雪琴, 袁丽. 肺炎支原体肺炎IL-2、sIL-2R、IL-6、IL-8检测[J]. 四川医学, 2012, 33(9): 1671-1672. [DOI]
|
| [16] |
王群. 小剂量IL-2对结缔组织病合并EB病毒、巨细胞病毒血症患者TH17/TREG失衡影响的研究[D/OL]. 山西医科大学, 2017. http://kns.cnki.net/kcms/detail/detail.aspx?filename=1017848235.nh&dbcode=CMFD&dbname=CMF-D2018&v=.
|
| [17] |
李成帅. 肺炎支原体合并EB病毒感染的临床研究及免疫分析[D/OL]. 大连医科大学, 2012. http://kns.cnki.net/kcms/detail/detail.aspx?filename=1013263259.nh&dbcode=CMFD&dbname=CMFD2014&v=.
|
| [18] |
Yong SC, Chen SJ, Boo NY. Incidence of nasal trauma associated with nasal prong versus nasal mask during continuous positive airway pressure treatment in very low birthweight infants:a randomised control study[J]. Arch Dis Child Fetal Neonatal Ed, 2005, 90(6): F480-F483.
[DOI]
|
| [19] |
吕慧, 贠国俊. 肺炎支原体感染儿童血清白细胞介素-6的水平分析[J]. 中国妇幼保健, 2013, 28(25): 4165-4166. [DOI]
|
| [20] |
张慧霞, 常晓悦, 王利军. IL-6与肺部炎性疾病关系最新进展[J]. 国际呼吸杂志, 2015, 35(1): 74-78. [DOI]
|
| [21] |
Deng MH, Lin CW, Sun YN, Zeng XL, Wen F. Role of E-selectin for diagnosing myocardial injury in paediatric patients with Mycoplasma pneumoniae pneumonia[J]. Ann Clin Biochem, 2017, 54(1): 49-54.
[DOI]
|
| [22] |
彭槐玉, 彭翠君, 李波, 游晓星. 肺炎支原体诱导单核细胞产生IL-6的分子机制[J]. 中国现代医生, 2008, 46(13): 60-61, 67. [DOI]
|
| [23] |
Tian F, Han B, Duan M. Serum tumor necrosis factor-alpha, interleukin-6 and galctin-3 concentrations in children with Mycoplasma pneumoniae pneumonia[J]. Zhongguo Dang Dai Er Ke Za Zhi, 2014, 16(10): 1001-1004.
[PubMed]
|
| [24] |
Carvalho WB, Johnston C, Fonseca MC. Acute bronchiolitis, an updated review[J]. Rev Assoc Med Bras, 2007, 53(2): 182-188.
[DOI]
|
| [25] |
李菁, 包军, 鲍一笑, 刘全华, 嵇若旭, 林芊. 肺炎支原体肺炎患儿肺泡灌洗液病菌量及其与Th1/Th2细胞免疫应答的关系[J]. 临床儿科杂志, 2015, 33(8): 681-685. [DOI]
|
| [26] |
Kang YM, Ding MJ, Han YL, Wang SF, Ma X, Li H. Th1/Th2 immune response in bronchoalveolar lavage fluid in children with severe Mycoplasma pneumoniae pneumonia[J]. Zhongguo Dang Dai Er Ke Za Zhi, 2011, 13(3): 188-190.
[PubMed]
|
| [27] |
王有鹏, 景伟超, 谭杰军. 儿童支原体肺炎IFN-γ、IL-4水平的中西医研究现状[J]. 中医药学报, 2014, 16(4): 133-135. [DOI]
|
| [28] |
Li W, Liu YJ, Zhao XL, Shang SQ, Wu L, Ye Q, Xu H. Th1/Th2 cytokine profile and its diagnostic value in Mycoplasma pneumoniae pneumonia[J]. Iran J Pediatr, 2016, 26(1): e3807.
[PubMed]
|
| [29] |
薛丽雯, 符辰潞, 庄一波. 肺炎支原体肺炎患儿免疫功能的变化[J]. 实用临床医药杂志, 2017, 21(21): 39-41. [URI]
|
| [30] |
Medjo B, Atanaskovic-Markovic M, Nikolic D, Radic S, Lazarevic I, Cirkovic I, Djukic S. Increased serum interleukin-10 but not interleukin-4 level in children with Mycoplsmma pneumonia pneumonia[J]. J Trop Pediatr, 2017, 63(4): 294-300.
[PubMed]
|
| [31] |
Wilke CM, Wei S, Wang L, Kryczek I, Kao J, Zou W. Dual biological effects of the cytokines interleukin-10 and interferon-γ[J]. Cancer Immunol Immunother, 2011, 60(11): 1529-1541.
[DOI]
|
| [32] |
Toyama M, Kudo D, Aoyagi T, Miyasaka T, Ishii K, Kanno E, Kaku M, Kushimoto S, Kawakami K. Attenuated accumulation of regulatory T cells and reduced production of interleukin 10 lead to the exacerbation of tissue injury in a mouse model of acute respiratory distress syndrome[J]. Microbiol Immunol, 2018, 62(2): 111-123.
[DOI]
|
| [33] |
Guo H, He Z, Li M, Wang T, Zhang L. Imbalance of peripheral blood Th17 and Treg responses in children with refractory Mycoplasma pneumoniae pneumonia[J]. J Infect Chemother, 2016, 22(3): 162-166.
[DOI]
|
| [34] |
杜许芳, 周炯英. Th17/Treg失衡在肺炎支原体肺炎患儿中的作用及其机制[J]. 临床与病理杂志, 2016, 36(12): 2017-2021. [DOI]
|
 2018, Vol. 13
2018, Vol. 13


