由细菌、病毒、真菌等多种病原微生物所致的感染性疾病一直严重威胁着人类的健康, 其中细菌所致感染尽管应用抗生素使之病死率下降, 然而耐药菌的不断出现、新现和再现传染病的流行仍然是人类健康的重大威胁[1]。细菌入侵后, 机体会产生积极的免疫应答来抵御或消灭细菌, 其中程序性细胞死亡(programmed cell death, PCD)在这一过程中具有重要作用。新近发现的Gasdermin (GSDM)家族被证实能通过参与PCD过程而影响细菌感染的发展, 本文就其研究现状进行总结。
1 细菌感染与抗细菌天然免疫天然免疫是宿主在进化过程中形成的天然防御机制, 是负责监视和清除致病菌的“第一道防线”, 主要由物理屏障、化学屏障、微生物屏障、吞噬细胞、免疫分子等组成, 其中吞噬细胞在天然免疫中起关键性作用。吞噬细胞主要分为中性粒细胞和单核-巨噬细胞。吞噬细胞能通过游走接近感染区域, 再依靠不同的Toll样受体识别不同的病原相关分子模式(pathogen-associated molecular pattern, PAMP), 之后将致病菌吞入形成吞噬体, 并与溶酶体融合成为吞噬溶酶体, 进而杀灭致病菌[2]。然而, 当细菌的毒力较强, 吞噬细胞无法完全杀灭被吞噬的细菌时, 吞噬细胞会发生细胞凋亡(apoptosis)或细胞焦亡(pyroptosis)等PCD。细菌感染分为胞内菌和胞外菌感染, 针对胞外菌感染, 天然免疫主要依靠吞噬细胞来杀灭和清除。而胞内菌感染时, 有些胞内菌在被吞噬细胞吞噬时会采取不同的策略抵抗或阻碍宿主吞噬细胞的吞噬, 甚至在被吞噬细胞吞噬后, 仍能积极抵抗杀伤作用, 在其中生存和繁殖, 这一现象被称为不完全吞噬(incomplete phagocytosis)。胞内菌避免被吞噬细胞杀伤的策略一般有:①在吞噬体与溶酶体融合之前, 胞内菌从吞噬体中逃逸至细胞质内无杀伤物质存在的区域, 避免进入吞噬溶酶体[2]。②阻止吞噬体与溶酶体融合, 在吞噬体内生存。③阻止吞噬溶酶体酸化, 不引发呼吸爆发(respiratory burst), 免受其产生的反应性氧中介物等强氧化物质的杀伤。④产生过氧化氢酶及超氧化物歧化酶, 有效清除H2O2、OH-和O2-, 在吞噬溶酶体中生存。⑤合成酪氨酸磷酸酯酶和丝氨酸激酶[3], 这两种酶的作用分别是去磷酸化和磷酸化, 它们共同调节细胞生命活动中的磷酸化水平[4], 而磷酸化水平的变化涉及生命活动中许多信号通路的激活或关闭, 细菌将这两种酶注入吞噬细胞内使其吞噬功能丧失[2]。细菌感染造成的损伤不但与细菌的毒力有关, 而且与宿主的免疫抵抗能力也有关系, 在细菌与宿主相互作用过程中, GSDM家族成员参与其中, 并起到了关键作用。
2 GSDM家族与抗细菌天然免疫 2.1 GSDM家族概况GSDM家族是最近被发现的有关PCD的蛋白家族, 人类与鼠类中的GSDM家族成员稍有不同(表 1)。在人类GSDM家族中, 成员主要分为6类, 分别为Gasdermin A(又名GSDMA或GSDM1), Gasdermin B(又名GSMDB、GSDML或PRO2521), Gasdermin C(又名GSDMC或MLZE), Gasdermin D(又名GSDMD、GSDMDC1或DFNA5L), Gasdermin E(又名GSDME或DFNA5)和Pejvakin(又名GSDMF、DFNB59或PJVK)。而在小鼠GSDM家族中, 没有GSDMB存在, 但却拥有3种GSDMA的同系物(GSDMA1、GSDMA2和GSDMA3)和4种GSDMC的同系物(GSDMC1、GSDMC2、GSDMC3和GSDMC4)[5]。
| Human GSDM family | Expression | Mouse GSDM family | Expression |
| GSDMA | Esophagus, lower gastrointestinal tract, mammary gland, skin, and stomach | GSDMA1 | Skin and the squamous epithelium of the stomach cardia |
| GSDMA2 | Skin | ||
| GSDMA3 | Epithelium of glandular stomach | ||
| GSDMB | Bronchial epithelium of asthmatic lungs, the epithelium of esophagus and gastrointestinal tract | Expression not reported or unknown | Expression not reported or unknown |
| GSDMC | Trachea, epithelial cells of the stomach and esophagus | GSDMC1-4 | Stomach, small intestine, cecum and colon |
| GSDMD | Esophagus, stomach and skin | GSDMD | Esophagus, stomach, skin, small intestine, cecum and colon |
| GSDME | Brain, heart, kidney and placenta | GSDME | Cochlea, thymus, colon, lung, brain, spleen and small intestine |
| GSDMF | Hair cells, supporting cells of the central nervous system, spiral ganglion neurons, spiral ganglion cells of the inner ear and the cell bodies of neurons | GSDMF | Brain, eye, ear, lung, heart, liver, kidney and small intestine |
① 人GSDMA主要在食管、下消化道、乳腺、皮肤和胃中表达; 小鼠GSDMA1在皮肤和胃贲门的鳞状上皮细胞中表达, GSDMA2在皮肤中表达, GSDMA3在胃上皮细胞中表达[6]。②GSDMB在哮喘患者肺支气管上皮、食管上皮和胃肠道上皮均有特异性表达[7]。③编码人GSDMC的基因在气管、脾脏和胃食管上皮细胞中表达, 而在小鼠中, 编码GSDMC的基因在胃、小肠、盲肠和结肠中表达[7]。④人GSDMF表达于毛细胞、中枢神经系统支持细胞、螺旋神经节神经元、内耳螺旋神经节细胞和神经元胞体[8]。小鼠GSDMF多表达于脑、眼、耳、肺、心脏、肝脏、肾和小肠[9]。⑤GSDMD多在人食管、胃和肠道中表达, 在小鼠肠道中也有表达。GSDMD不仅在宿主防御中发挥作用, 并且关于其介导焦亡的作用常被报道[6]。⑥人GSDME在脑、心、肾、胎盘中均有表达, 小鼠GSDME表达于耳蜗、胸腺、结肠、肺、脑、脾和小肠[10]。GSDME在细胞凋亡和焦亡中也发挥着重要作用[11]。
2.1.2 GSDM家族的主要生物学功能① 人GSDMA和小鼠GSDMA3的氨基端(N-terminal, N端)结构域在293T等细胞中过表达时会在质膜上打孔, 产生细胞焦亡特征。当GSDMA3的N端结构发生突变时, 小鼠发生脱发、皮肤炎症、皮肤角化病、畸形生长的风险上升[5, 11]。②GSDMB的膜结合偏好与其他GSDM家族成员不同。GSDMB的全长和N端结构域均可与磷酸肌醇和糖脂类硫苷脂结合。与硫苷脂结合的能力表明GSDMB可能与细胞膜的外侧脂质相互作用, 这与其他GSDM家族成员不同[12]。③GSDMC被认为是一种转录因子, 它不能通过炎症或细胞凋亡相关的天冬氨酸特异性半胱氨酸蛋白酶(cysteinyl aspartate specific proteinase, caspase)被激活。GSDMC最初被命名为黑色素瘤衍生的亮氨酸拉链, 因为在其羧基端(C-terminal, C端)结构域存在一个这样的结构, 这表明GSDMC可能识别细胞核中的特定DNA序列, 并可能在细胞核和细胞质之间传输信号[8]。④GSDMF是一种与人类和小鼠听力损伤相关的蛋白质。GSDMF的N端结构域2种错义突变会使听觉神经元传递听觉信号受损, 导致耳聋[9]。⑤GSDMD具有诱导PCD和引发炎症的能力, 主要是在炎性小体信号传导和焦亡中起作用。GSDMD是炎性小体相关caspase的底物, 当GSDMD被caspase切割后, GSDMD的N端结构域活化, 具有在宿主细胞膜上打孔的能力, 既能使细胞内外钠-钾离子浓度失去平衡, 又能诱导细胞因子等释放和引发PCD, 并与炎性小体的激活相关[5, 11]。⑥GSDME可通过caspase-3的切割, 使其N端结构域活化, 在细胞膜上打孔, 诱导细胞焦亡, 该结构域的过表达可导致293T细胞等产生细胞焦亡特征。有进一步的研究表明, 转染含有编码人为截短的GSDME质粒会导致HEK293T细胞中活性氧(reactive oxygen species, ROS)水平升高, 引发细胞凋亡和坏死性细胞死亡[11]。因为GSDM家族在宿主与细菌的博弈中被两者所影响, 所以研究其在细菌感染中的作用机制和生物学意义能为细菌感染性疾病的新药研发和临床治疗提供新的思路。
2.2 GSDM家族在PCD中的作用除GSDMF以外, GSDM家族成员都具有保守的双结构域序列:N端结构域和C端结构域。GSDM家族成员(除了GSDMF)被半胱天冬氨酸蛋白酶caspase切割后, 均能使其N端活化, 从而具有在细胞膜上打孔的能力, 使细胞释放白细胞介素(interleukin, IL)1β和IL-18, 参与炎症反应, 在PCD中发挥重要作用[13]。该过程与下述有关:①细菌的侵入途径、所携带的毒力基因种类及毒力基因编码产物的作用方式; ②机体的免疫系统状况。以往认为在caspase家族中, caspase-2、3、6、7、8、9、10与细胞凋亡过程有关, caspase-1、4、5、11与炎症反应有关[14], 然而新近研究显示caspase家族在PCD中的作用可能并非如此[15-16, 21]。
在PCD中, 细胞凋亡是一种重要的细胞死亡类型。细胞凋亡是一种主动过程, 它涉及一系列的基因激活、表达、调控等。细胞凋亡是多基因严格控制的过程, 这些基因在种属之间非常保守, 如Bcl-2家族、caspase家族、癌基因c-myc、抑癌基因p53等。研究表明, 切割GSDME的caspase-3在天然或非天然细胞凋亡中也发挥着不可替代的作用[17], 例如caspase-3能通过MAPK中的JNK子途径发挥作用:在JNK双磷酸化后激活JNK通路, 促进转录因子复合物AP-1活性并伴随多种凋亡蛋白产生, 之后激活线粒体Bcl-2家族等, 释放细胞色素C, 细胞色素C和caspase-9或凋亡蛋白酶激活因子(Apaf-1)结合, 作用于caspase-3, caspase-3与凋亡底物结合, 引起细胞凋亡; 并且在诸如此类的凋亡过程中, 都能检测到含量上升的活性化GSDME[15]。近期有报道显示, caspase-1在GSDMD缺乏的细胞中, 能引发细胞凋亡[16]。此外, GSDMA3在肿瘤坏死因子α(tumor necrosis factor α, TNF-α)所诱导的角化细胞中凋亡信号是必需的, GSDMA3通过直接增强caspase-3表达, 导致了毛囊角化细胞凋亡[18]。
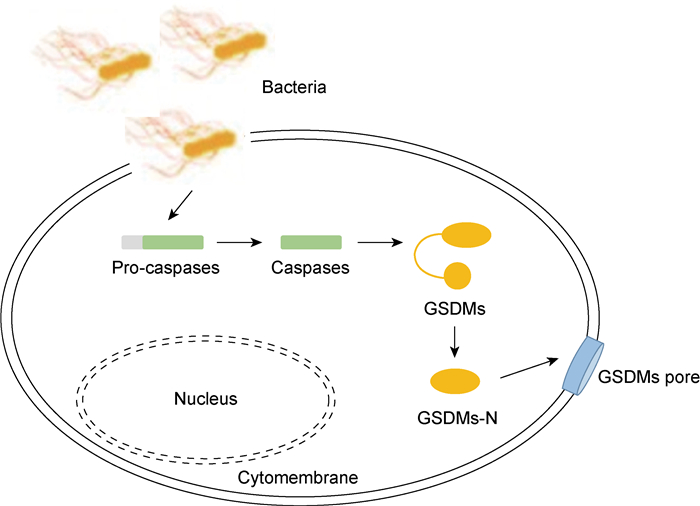
细胞焦亡是一种近年来发现的新的PCD, 表现为细胞不断胀大直至细胞膜破裂, 导致细胞内容物和大量与炎症密切相关的促炎症因子释放, 在抗感染中发挥重要作用。细胞焦亡的引发主要有2种途径。①经典途径:在PAMP和损伤相关分子模式(damage-associated molecular pattern, DAMP)的作用下, 胞质内感受器(NOD-like receptors, NLR)蛋白家族成员, 如NLRP3(NOD-like receptor family, pyrin domain containing 3)炎性小体[19]等会识别这些信号, 通过衔接蛋白ASC(apoptosis-associated speck-like protein with a caspase-recruitment domain)与caspase-1前体结合, 激活caspase-1, caspase-1切割GSDMD, 使其N端活性化而拥有在细胞质膜上打孔的能力, 释放细胞内容物, 从而激活细胞焦亡; 同时活化的caspase-1对IL-1β和IL-18的前体进行切割, 使IL-1β和IL-18活性化, 其释放至胞外后募集炎症细胞聚集。②非经典途径:caspase其他家族成员如caspase-4、5、11的前体在脂多糖等作用下被活化, 活化的caspase-4、5、11切割GSDMD, 诱导焦亡发生[20]; 另一方面, 促进caspase-1活化, 对炎症因子IL-1β和IL-18的前体进行切割, 造成炎症反应。除了GSDMD以外, GSDME也被证实能在caspase-3的特异性切割作用下, 其N端活性化, 引起细胞焦亡[21]。研究发现, 不但在鼠髓源巨噬细胞和293T细胞这类能表达GSDME的细胞中发现了焦亡现象, 而且像HeLa细胞这类不能表达GSDME的细胞, 在经过转染一种编码GSDME的质粒后, 也能发现焦亡现象[22]。最近一项研究表明, 腺苷三磷酸(adenosine triphosphate, ATP)作为典型的激活因子诱导巨噬细胞内NLRP3炎性小体活化, 导致caspase-1/ GSDMD介导的焦亡, 然而当NLRP3通路被感染性疾病阻断时, ATP能通过caspase-3/GSDME诱导巨噬细胞焦亡[23](图 1)。研究发现, GSDMD和GSDME的N端不但能引发细胞焦亡, 而且能使线粒体膜渗透化, 释放细胞色素C和caspase-3前体等与凋亡相关的因子, 激活凋亡小体[24]。
|
| 图 1 GSDM家族成员经caspase切割后的活性化 Fig. 1 GSDM family are activated after caspase cleavage |
GSDMA3能通过自我调节, 控制自身组分缺失并靶向线粒体, 引起细胞自噬。GSDMA3的N端具有促自噬活性, 而其C端则具有抑制自噬活性的功能。GSDMA3突变体通过失去整个C端结构域来释放N端结构域固有的促自噬活性, 然后GSDMA3的N末端结构域与Hsp90/Hsp70复合物相关联, 通过线粒体导入受体Tom70传递给线粒体。在那里它与线粒体伴侣Trap1相互作用并诱导线粒体通透性转换孔开放, 生产线粒体ROS, 释放细胞色素C, 最终导致细胞自噬[25]。
中性粒细胞胞外诱捕网(neutrophil extracellular traps, NETs)的形成, 可导致一种形式的细胞死亡, 称为NETosis[26]。这是一种新发现的PCD方式, 近年来的一些研究已经发现了GSDMD介导的NETosis机制。GSDMD的C端结构域(也称为p20片段)与N端结构域(也称为p30片段)之间的连接裂解后, 释放了N端结构域, 该结构域寡聚形成细胞膜上的孔。这些小孔增加了细胞膜的通透性, 促进NETs或炎症细胞因子的释放, 从而引发炎症反应的级联反应[27]。
有研究表明, 缺乏GSDMD/caspase-8的调控会促进细胞坏死性凋亡水平[28]。在293T等特殊细胞中, GSDME能在TNF等诱导下, 经caspase-3切割, 使得细胞从凋亡状态迅速转向继发性坏死/焦亡转变[29], 暗示了GSDM家族参与的各种PCD之间可能存在某种联系。GSDME还被猜测能在PCD早期通过促进细胞膜通透性, 负调控凋亡细胞分裂成更小的膜结合小泡, 有利于细胞内促炎性物质的释放[30]。
2.3 GSDM家族在细菌感染中的作用近年来, 有关GSDM家族成员在细菌入侵宿主并规避免疫防御机制的研究已为热点, 其在部分细菌中的作用已得到证实。
沙门菌(Salmonella)感染能够引起宿主细胞焦亡。沙门菌感染巨噬细胞后, 其鞭毛蛋白等能引发caspase-1切割GSDMD, 使其N端活性化, 从而在细胞膜上打孔, 引发细胞焦亡[31]; 沙门菌感染中性粒细胞时会引发非经典炎症信号通路, 并引起依赖GSDMD的NETosis, 而GSDMD将这两种细胞死亡方式联系起来[32]。人GBP1能够在沙门菌感染时增强caspase-4的激活, 并导致依赖GSDMD的细胞焦亡, 促进抗细菌天然免疫[33]。沙门菌质粒毒力基因spv在沙门菌侵入宿主机体和规避宿主免疫防御的过程中起到了关键作用。本课题组近阶段研究显示, spv可影响宿主细胞GSDM活化, 进而干预细菌感染的进程。沙门菌spv包括调控基因spvR和4个结构基因spvA、spvB、spvC和spvD[34]。spvB编码的效应蛋白SpvB具有二磷酸腺苷-核糖基转移酶活性, 它能共价修饰G-肌动蛋白(G-actin)单体, 从而抑制其聚合形成F-肌动蛋白(F-actin), 最终影响细胞骨架解聚[34]。本课题组前期研究证实SpvB还能通过抑制自噬体的形成, 阻止宿主细胞通过自噬清除细菌[35]。spvC编码的效应蛋白SpvC能通过抑制宿主体内的MAPK信号途径激活, 从而降低促炎症细胞因子和趋化因子的水平, 抑制炎症反应, 促进沙门菌的全身播散[36]。spvD编码的效应蛋白SpvD则具有caspase活性, 通过抑制核因子κB(nuclear factor κB, NF-κB)信号转导通路从而抑制炎症反应, 促进沙门菌的全身播散[37]。
耶尔森菌(Yersinia)蛋白J(YopJ)是由耶尔森菌分泌到宿主细胞中的一种Ⅲ型分泌系统(T3SS)效应蛋白, 近年来YopJ被证实能够通过抑制巨噬细胞等的MAPK通路和NF-κB通路等, 调控细胞死亡。耶尔森菌能通过YopJ抑制TAK1来抑制TNF等细胞因子的表达, 阻止IL-1前体的产生, 并在TAK1抑制期间, 通过caspase-8的激活, 切割小鼠巨噬细胞中的GSDMD和GSDME, 导致N端活化, 在细胞膜上打孔及释放内容物, 从而使细胞焦亡。耶尔森菌通过分泌YopJ, 在抑制MAPK途径和阻止IL-1前体释放的同时, 主动引发细胞焦亡, 从而在杀死巨噬细胞的同时抑制炎症反应, 破坏宿主的免疫防御[38]。人类巨噬细胞具有抵抗YopJ介导的细胞焦亡的能力, 因此与啮齿类动物宿主相比, 人类对耶尔森菌感染有更高的敏感性。
肠出血性大肠埃希菌(Enterohemorrhagic escherichia coli, EHEC)分泌的志贺毒素2(Stx2)能激活人巨噬细胞THP-1中的caspase-4、GSDMD和NLRP3炎性小体, 但不激活缺乏Stx受体CD77的小鼠巨噬细胞。Stx2介导的IL-1β分泌和细胞焦亡依赖于线粒体中富含的线粒体ROS以及GSDMD的裂解。抑制caspase-4激活, ROS生成及GSDMD缺陷会显著减少Stx2介导的IL-1β生产和细胞焦亡。NLRP3炎性小体在Stx2诱导的GSDMD裂解中发挥重要作用, 在NLRP3缺失的THP-1细胞中, 这些反应显著降低。Stx2会激活NLRP3炎性小体上游的非经典炎性小体和线粒体ROS, 促进细胞因子成熟和细胞吞噬。EHEC分泌的Stx2在其脂多糖的辅助作用下, 促进IL-1β和TNF-α的生成, 并诱导GSDMD介导的细胞焦亡, 引发剧烈的炎症反应, 对机体造成严重损伤[39]。
新洋葱伯克霍尔德菌(Burkholderia cenocepacia)[40]是一种革兰阴性机会致病菌, 可引起囊性纤维化病患者发生严重的慢性肺部感染。新洋葱伯克霍尔德菌采用一种被命名为TecA的非VgrG的Ⅵ型分泌系统(T6SS), 通过抑制Rho GTP酶活性, 导致肌动蛋白细胞骨架的解聚, 从而在巨噬细胞中存活。TecA和其他细菌同源物携带caspase样催化三联物, 通过在GTP酶Ⅰ型开关区域使保守的天冬酰胺去酰胺化, 从而导致Rho GTP酶失活。RhoA脱氨会诱导caspase-1活化, 该活化由家族性地中海热病蛋白Pyrin介导, 并最终使GSDMD被切割后活性化, 引发PCD, 促进炎症反应。新洋葱伯克霍尔德菌通过分泌TecA主动介导PCD, 引发炎症使机体免受因细菌感染造成的致命损伤, 从而与宿主达到共生或互利的状态[41]。
新凶手弗朗西斯菌(Francisella novicida)[42]能主动通过AIM2炎性小体活化GSDMD, 引发细胞焦亡, 抑制环GMP-AMP合酶(cyclic GMP-AMP synthase, cGAS)驱动Ⅰ型干扰素的产生, 抵抗后者对其杀伤作用。有报道证实β干扰素(IFN-β)对新凶手弗朗西斯菌感染的反应在GSDMD缺陷小鼠中升高。AIM2炎性小体激活的GSDMD在介导细胞焦亡的同时, 还能导致细胞内外钾离子浓度失衡, 最终耗尽细胞内钾离子。这种钾离子外排对抑制cGAS依赖的IFN-β产生是充分且必要的[43]。
除此之外, GSDM家族在金黄色葡萄球菌感染(Staphylococcus aureus)造成的骨损伤[44]以及在志贺菌(Shigella)和肺炎链球菌(Streptococcus pneumoniae)等造成的细菌感染[45]引发的PCD中都起到了重要作用。
3 结语研究表明, GSDM家族介导的宿主PCD在部分细菌入侵造成的感染中扮演了重要的角色。PCD是一种宿主机体在细菌入侵时重要的抵抗方式, 它拥有提供抗原信息、围困细胞内细菌使之不能离开细胞残体和淘汰寄生体等功能, 因此细菌在感染机体时一般会避免PCD。然而, 迄今为止已发现众多病原体能在感染机体时主动引发PCD[38-39, 41, 43, 46]。与上述PCD过程相关的GSDM家族则在细胞凋亡、细胞焦亡及继发性坏死等方面起着无可替代的作用[31-46]。研究细菌感染与GSDM家族介导PCD之间的关系, 能够为此类疾病的临床医治、预防以及新药研发提供新思路。
| [1] |
翟爱霞, 窦豆, 羊正纲, 张建业, 漆智, 闫章才. 2009—2018年度国家自然科学基金医学病原微生物与感染领域细菌相关项目申请与资助情况分析[J]. 微生物与感染, 2019, 14(2): 65-71. [URI]
|
| [2] |
贾文祥. 医学微生物学[M]. 第3版. 北京: 人民卫生出版社, 2015: 68-79.
|
| [3] |
Zhou R, Chen Z, Hao D, Wang Y, Zhang Y, Yi X, Lyu LD, Liu H, Zou Q, Chu Y, Ge B, Yan D. Enterohemorrhagic Escherichia coli Tir inhibits TAK1 activation and mediates immune evasion[J]. Emerg Microbes Infect, 2019, 8(1): 734-748.
[DOI]
|
| [4] |
薛闯, 张萌, 陈丽杰. 激酶组学在原核生物中的研究进展[J]. 微生物学杂志, 2017, 37(5): 1-7. [DOI]
|
| [5] |
Feng S, Fox D, Man SM. Mechanisms of gasdermin family members in inflammasome signaling and cell death[J]. J Mol Biol, 2018, 430(18 Pt B): 3068-3080.
[URI]
|
| [6] |
Saeki N, Kuwahara Y, Sasaki H, Satoh H, Shiroishi T. Gasdermin (Gsdm) localizing to mouse Chromosome 11 is predominantly expressed in upper gastrointestinal tract but significantly suppressed in human gastric cancer cells[J]. Mamm Genome, 2000, 11(9): 718-724.
[DOI]
|
| [7] |
Saeki N, Usui T, Aoyagi K, Kim DH, Sato M, Mabuchi T, Yanagihara K, Ogawa K, Sakamoto H, Yoshida T, Sasaki H. Distinctive expression and function of four GSDM family genes (GSDMA-D) in normal and malignant upper gastrointestinal epithelium[J]. Genes Chromosomes Cancer, 2009, 48(3): 261-271.
[DOI]
|
| [8] |
Watabe K, Ito A, Asada H, Endo Y, Kobayashi T, Nakamoto K, Itami S, Takao S, Shinomura Y, Aikou T, Yoshikawa K, Matsuzawa Y, Kitamura Y, Nojima H. Structure, expression and chromosome mapping of MLZE, a novel gene which is preferentially expressed in metastatic melanoma cells[J]. Jpn J Cancer Res, 2001, 92(2): 140-151.
[DOI]
|
| [9] |
Delmaghani S, del Castillo FJ, Michel V, Leibovici M, Aghaie A, Ron U, Van Laer L, Ben-Tal N, Van Camp G, Weil D, Langa F, Lathrop M, Avan P, Petit C. Mutations in the gene encoding pejvakin, a newly identified protein of the afferent auditory pathway, cause DFNB59 auditory neuropathy[J]. Nat Genet, 2006, 38(7): 770-778.
[DOI]
|
| [10] |
van Laer L, Huizing EH, Verstreken M, van Zuijlen D, Wauters JG, Bossuyt PJ, Van de Heyning P, McGuirt WT, Smith RJ, Willems PJ, Legan PK, Richardson GP, Van Camp G. Nonsyndromic hearing impairment is associated with a mutation in DFNA5[J]. Nat Genet, 1998, 20(2): 194-197.
[DOI]
|
| [11] |
Kovacs SB, Miao EA. Gasdermins: effectors of pyroptosis[J]. Trends Cell Biol, 2017, 27(9): 673-684.
[DOI]
|
| [12] |
Chao KL, Kulakova L, Herzberg O. Gene polymorphism linked to increased asthma and IBD risk alters gasdermin-B structure, a sulfatide and phosphoinositide binding protein[J]. Proc Natl Acad Sci USA, 2017, 114(7): E1128-E1137.
[DOI]
|
| [13] |
Aglietti RA, Dueber EC. Recent insights into the molecular mechanisms underlying pyroptosis and gasdermin family functions[J]. Trends Immunol, 2017, 38(4): 261-271.
[DOI]
|
| [14] |
Logue SE, Martin SJ. Caspase activation cascades in apoptosis[J]. Biochem Soc Trans, 2008, 36(Pt 1): 1-9.
[URI]
|
| [15] |
梁先敏, 杨克敌. Caspase和JNK/SAPK、p38 MAPK与细胞凋亡[J]. 国外医学·卫生学分册, 2008, 35(1): 5-10. [URI]
|
| [16] |
Tsuchiya K, Nakajima S, Hosojima S, Thi Nguyen D, Hattori T, Manh Le T, Hori O, Mahib MR, Yamaguchi Y, Miura M, Kinoshita T, Kushiyama H, Sakurai M, Shiroishi T, Suda T. Caspase-1 initiates apoptosis in the absence of gasdermin D[J]. Nat Commun, 2019, 10(1): 2091.
[DOI]
|
| [17] |
Chen KW, Demarco B, Heilig R, Shkarina K, Boettcher A, Farady CJ, Pelczar P, Broz P. Extrinsic and intrinsic apoptosis activate pannexin-1 to drive NLRP3 inflammasome assembly[J]. EMBO J, 2019, 38(10): e101638.
[DOI]
|
| [18] |
Lei M, Gao X, Yang L, Yang T, Lian X. Gsdma3 gene is needed for the induction of apoptosis-driven catagen during mouse hair follicle cycle[J]. Histochem Cell Biol, 2011, 136(3): 335-343.
[DOI]
|
| [19] |
杨斯迪, 邓奇峰, 黄瑞, 吴淑燕. 炎性小体激活与细胞焦亡的研究进展[J]. 微生物与感染, 2017, 12(3): 192-196. [DOI]
|
| [20] |
Lim Y, Kumar S. A single cut to pyroptosis[J]. Oncotarget, 2015, 6(35): 36926-36927.
[URI]
|
| [21] |
Yu J, Li S, Qi J, Chen Z, Wu Y, Guo J, Wang K, Sun X, Zheng J. Cleavage of GSDME by caspase-3 determines lobaplatin-induced pyroptosis in colon cancer cells[J]. Cell Death Dis, 2019, 10(3): 193.
[DOI]
|
| [22] |
Wang Y, Gao W, Shi X, Ding J, Liu W, He H, Wang K, Shao F. Chemotherapy drugs induce pyroptosis through caspase-3 cleavage of a gasdermin[J]. Nature, 2017, 547(7661): 99-103.
[DOI]
|
| [23] |
Zeng CY, Li CG, Shu JX, Xu LH, Ouyang DY, Mai FY, Zeng QZ, Zhang CC, Li RM, He XH. ATP induces caspase-3/gasdermin E-mediated pyroptosis in NLRP3 pathway-blocked murine macrophages[J]. Apoptosis, 2019, 24(9-10): 703-717.
[DOI]
|
| [24] |
Rogers C, Erkes DA, Nardone A, Aplin AE, Fernandes-Alnemri T, Alnemri ES. Gasdermin pores permeabilize mitochondria to augment caspase-3 activation during apoptosis and inflammasome activation[J]. Nat Commun, 2019, 10(1): 1689.
[DOI]
|
| [25] |
Qiu S, Liu J, Xing F. 'Hints' in the killer protein gasdermin D: unveiling the secrets of gasdermins driving cell death[J]. Cell Death Differ, 2017, 24(4): 588-596.
[DOI]
|
| [26] |
Demers Mélanie, Wong Siu Ling, Martinod Kimberly, Gallant Maureen, Cabral Jessica E, Wang Yanming, Wagner Denisa D. Priming of neutrophils toward NETosis promotes tumor growth[J]. Oncoimmunology, 2016, 5(5): e1134073.
[DOI]
|
| [27] |
Pandeya A, Li L, Li Z, Wei Y. Gasdermin D (GSDMD) as a new target for the treatment of infection[J]. Medchemcomm, 2019, 10(5): 660-667.
[DOI]
|
| [28] |
Yang C, Sun P, Deng M, Loughran P, Li W, Yi Z, Li S, Zhang X, Fan J, Billiar TR, Scott MJ. Gasdermin D protects against noninfectious liver injury by regulating apoptosis and necroptosis[J]. Cell Death Dis, 2019, 10(7): 481.
[DOI]
|
| [29] |
Rogers C, Fernandes-Alnemri T, Mayes L, Alnemri D, Cingolani G, Alnemri ES. Cleavage of DFNA5 by caspase-3 during apoptosis mediates progression to secondary necrotic/pyroptotic cell death[J]. Nat Commun, 2017, 8: 14128.
[DOI]
|
| [30] |
Tixeira R, Shi B, Parkes MAF, Hodge AL, Caruso S, Hulett MD, Baxter AA, Phan TK, Poon IKH. Gasdermin E does not limit apoptotic cell disassembly by promoting early onset of secondary necrosis in Jurkat T cells and THP-1 monocytes[J]. Front Immunol, 2018, 9: 2842.
[DOI]
|
| [31] |
Man SM, Kanneganti TD. Gasdermin D: the long-awaited executioner of pyroptosis[J]. Cell Res, 2015, 25(11): 1183-1184.
[DOI]
|
| [32] |
Fisch D, Bando H, Clough B, Hornung V, Yamamoto M, Shenoy AR, Frickel EM. Human GBP1 is a microbe-specific gatekeeper of macrophage apoptosis and pyroptosis[J]. EMBO J, 2019, 38(13): e100926.
[URI]
|
| [33] |
Chen KW, Monteleone M, Boucher D, Sollberger G, Ramnath D, Condon ND, von Pein JB, Broz P, Sweet MJ, Schroder K. Noncanonical inflammasome signaling elicits gasdermin D-dependent neutrophil extracellular traps[J]. Sci Immunol, 2018, 3(26): eaar6676.
[DOI]
|
| [34] |
孙兰清, 左玲莉, 杨斯迪, 黄瑞, 吴淑燕. 沙门菌致病的奥秘[J]. 科学(上海), 2019, 71(1): 42-46. [URI]
|
| [35] |
Chu Y, Gao S, Wang T, Yan J, Xu G, Li Y, Niu H, Huang R, Wu S. A novel contribution of spvB to pathogenesis of Salmonella typhimurium by inhibiting autophagy in host cells[J]. Oncotarget, 2016, 7(7): 8295-8309.
[PubMed]
|
| [36] |
Haneda T, Ishii Y, Shimizu H, Ohshima K, Iida N, Danbara H, Okada N. Salmonella type Ⅲ effector SpvC, a phosphothreonine lyase, contributes to reduction in inflammatory response during intestinal phase of infection[J]. Cell Microbiol, 2012, 14(4): 485-499.
[DOI]
|
| [37] |
Rolhion N, Furniss RC, Grabe G, Ryan A, Liu M, Matthews SA, Holden DW. Inhibition of nuclear transport of NF-κB p65 by the Salmonella type Ⅲ secretion system effector SpvD[J]. PLoS Pathog, 2016, 12(5): e1005653.
[DOI]
|
| [38] |
Sarhan J, Liu BC, Muendlein HI, Li P, Nilson R, Tang AY, Rongvaux A, Bunnell SC, Shao F, Green DR, Poltorak A. Caspase-8 induces cleavage of gasdermin D to elicit pyroptosis during Yersinia infection[J]. Proc Natl Acad Sci USA, 2018, 115(46): E10888-E10897.
[DOI]
|
| [39] |
Platnich JM, Chung H, Lau A, Sandall CF, Bondzi-Simpson A, Chen HM, Komada T, Trotman-Grant AC, Brandelli JR, Chun J, Beck PL, Philpott DJ, Girardin SE, Ho M, Johnson RP, MacDonald JA, Armstrong GD, Muruve DA. Shiga toxin/lipopolysaccharide activates caspase-4 and gasdermin D to trigger mitochondrial reactive oxygen species upstream of the NLRP3 inflammasome[J]. Cell Rep, 2018, 25(6): 1525-1536.
[DOI]
|
| [40] |
苏智军, 明德松. 重型肝炎患者痰Burkholderia cenocepacia 39种耐药基因的研究[J]. 中华医院感染学杂志, 2009, 19(20): 2690-2692, 2703. [URI]
|
| [41] |
Aubert DF, Xu H, Yang J, Shi X, Gao W, Li L, Bisaro F, Chen S, Valvano MA, Shao F. A Burkholderia type Ⅵ effector deamidates Rho GTPases to activate the pyrin inflammasome and trigger inflammation[J]. Cell Host Microbe, 2016, 19(5): 664-674.
[DOI]
|
| [42] |
Price AA, Sampson TR, Ratner HK, Grakoui A, Weiss DS. Cas9-mediated targeting of viral RNA in eukaryotic cells[J]. Proc Natl Acad Sci USA, 2015, 112(19): 6164-6169.
[DOI]
|
| [43] |
Feltham R, Vince JE. Ion man: GSDMD punches pores to knock out cGAS[J]. Immunity, 2018, 49(3): 379-381.
[DOI]
|
| [44] |
Zhu X, Zhang K, Lu K, Shi T, Shen S, Chen X, Dong J, Gong W, Bao Z, Shi Y, Ma Y, Teng H, Jiang Q. Inhibition of pyroptosis attenuates Staphylococcus aureus-induced bone injury in traumatic osteomyelitis[J]. Ann Transl Med, 2019, 7(8): 170.
[DOI]
|
| [45] |
Kayagaki N, Stowe IB, Lee BL, O'Rourke K, Anderson K, Warming S, Cuellar T, Haley B, Roose-Girma M, Phung QT, Liu PS, Lill JR, Li H, Wu J, Kummerfeld S, Zhang J, Lee WP, Snipas SJ, Salvesen GS, Morris LX, Fitzgerald L, Zhang Y, Bertram EM, Goodnow CC, Dixit VM. Caspase-11 cleaves gasdermin D for non-canonical inflammasome signalling[J]. Nature, 2015, 526(7575): 666-671.
[DOI]
|
| [46] |
Lin Y, Jiao Y, Yuan Y, Zhou Zu, Zheng Y, Xiao Ji, Li C, Chen Z, Cao P. Propionibacterium acnes induces intervertebral disc degeneration by promoting nucleus pulposus cell apoptosis via the TLR2/JNK/ mitochondrial-mediated pathway[J]. Emerg Microbes Infect, 2018, 7(1): 1.
[DOI]
|
 2019, Vol. 14
2019, Vol. 14


